Конспект "Карбонові кислоти, їх поширення в природі та класифікація".
Тема уроку №28: «Карбонові кислоти, їх поширення в природі та класифікація. Карбоксильна характеристична (функціональна) група. Склад, будова молекул насичених одноосновних карбонових кислот, їхня загальна та структурні формули, ізомерія, систематична номенклатура і фізичні властивості».
Мета:
освітня – сприяти розвитку знань учнів про карбонільні органічні сполуки на прикладі карбонових кислот; формувати знання про карбоксильну функціональну групу на прикладі карбонових кислот; ознайомити учнів зі структурною й електронною формулами оцтової кислоти; показати зв’язок між функціональною карбоксильною групою та фізичними властивостями карбонових кислот; формувати уявлення про гомологічний ряд одноосновних карбонових кислот, ізомерію і структурні формули.
розвиваюча - допомогти розвивати спостережливість, мислення, навчки складати хімічні формули та проводити хімічний експеримент.
виховна – сприяти виховуванню наукового світогляду.
Формування ключових компетентностей: спілкування державною мовою, основні компетентності у природничих науках і технологіях, ініціативність і підприємливість, уміння вчитися впродовж життя, соціальна та громадянська компетентності, обізнаність та самовираження у сфері культури, екологічна грамотність і здорове життя.
Наскрізні лінії: «Екологічна безпека і сталий розвиток».
Обладнання: зошит, підручник.
Основні поняття та терміни: карбонові кислоти, масляна, мурашина, оцтова, валеріанова, естери.
Методи та прийоми: хімічний диктант, лабораторна робота, демонстрація, бесіда, розповідь, пояснення, виконання вправ.
Тип уроку: комбінований.
Дата проведення: ___________
Клас: 10
Структура уроку
І.Етап орієнтації, мотивації діяльності.
ІІ. Етап контролю домашнього завдання.
ІІІ. Етап цілевизначення та планування.
ІV.Етап цілереалізації.
V. Рефлексивно-оцінювальний етап.
V. Етап повідомлення домашнього завдання.
Хід уроку.
І.Етап орієнтації, мотивації діяльності.
Привітання з класом, налаштування на робочий настрій.
ІІ. Етап контролю домашнього завдання. Усне опитування.
1. Хімічні властивості альдегідів.
2. Добування альдегідів.
3. Застосування альдегідів
Актуалізація опорних знань учнів. Хімічний диктант
Зобразіть структурну формулу речовини:
2-метилпропан, пропанол, 2-бутен, 2-метил-2-бутен, 2-метил-1-пропанол, бутаналь, етиловий спирт, 1,1-дихлоретан, метан, 3,3-диметилпентан, пропаналь.
ІІІ. Етап цілевизначення та планування.
«Мозковий штурм»


На столі на тарілці лежать яблука, мандарини, апельсини, лимони.
Вчитель (показує на фрукти). Як ви думаєте, що об'єднує ось ці смачні продукти? Правильно, в них є кислоти - фруктові з класу органічних карбонових кислот. А які асоціації виникають у вас при згадуванні слова «кислота»?
Отже, сьогодні ми маємо з’ясувати, які ж таки речовини, що називаються органічними кислотами? Які властивості вони мають? Де застосовуються?
ІV.Етап цілереалізації.
Даємо визначення органічним кислотам –карбоновим.
Карбонові кислоти – органічні оксигеновмісні сполуки, в молекулах яких вуглеводнева група сполучена з функціональною карбоксильною групою. Наводимо приклади.
CH3 COOH – оцтова кислота
 HCOOH – мурашина кислота.
HCOOH – мурашина кислота.
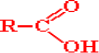
Загальна формула карбонових кислот:
Функціональна карбоксильна група -COOH
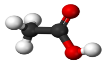 Записуємо структурну формулу карбоксильної функціональної групи, пояснюємо її будову.
Записуємо структурну формулу карбоксильної функціональної групи, пояснюємо її будову.
Записуємо молекулярну і структурну формули оцтової кислоти.
Молекулярна формула Структурна формула
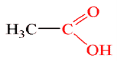 CH3COOH
CH3COOH
Класифікація карбонових кислот
![]() За кількістю карбоксильних груп
За кількістю карбоксильних груп
![]()
![]()
одноосновні двохосновні багатоосновні
(монокарбонові) (дикарбонові) (лимонна)
R – COOH R (COOH)2
(щавлева)
![]()
![]() За будовою вуглеводневого радикалу
За будовою вуглеводневого радикалу
![]()
насичені ненасичені ароматичні
СН3 – СН2 – СООН СН2 = СН – СООН С6Н5СООН
пропанова к – та акрилова к – та бензоатна к - та
Номенклатура карбонових кислот
|
Формула |
Назва |
|
|
систематична |
тривіальна |
|
|
HCOOH |
Метанова |
Мурашина |
|
CH3COOH |
Етанова |
Оцтова |
|
C2H5COOH |
Пропанова |
Пропіонова |
|
C3H7COOH |
Бутанова |
Масляна |
|
C4H9COOH |
Пентанова |
Валеріанова |
|
C5HnCOOH |
Гексанова |
Капронова |
|
C15H31COOH |
Пентадеканова |
Пальмітинова |
|
C17H35COOH |
Гептадеканова |
Стеаринова |
Ізомерія карбонових кислот
- Ізомерія карбонового ланцюга у вуглеводневому радикалі
(структурна ізомерія)
СН3 – СН2 - СН2 – СН2 – СООН пентанова к – та
СН3 – СН – СН2 – СООН 3 – метилбутанова к – та
│
СН3
- Міжкласова ізомерія
Одноосновним карбоновим кислотам ізомерні естри
СН3 – СН2 – СООН пропанова к – та
![]()
![]() О
О
![]() СН3 – С оцтовометиловий естер
СН3 – С оцтовометиловий естер
О – СН3
З’ясовуємо фізичні властивості карбонових кислот.
Оцтова кислота – безбарвна рідина, летка, має різкий специфічний запах, змішується з водою в будь-яких пропорціях, розчин кислий на смак;
- за t < 170 С кристалізується (“крижана кислота “);
- 3-9% водний розчин – столовий оцет;
- 86% водний розчин - оцтова есенція
Серед карбонових кислот відсутні газоподібні речовини. Чому? Це пов'язано з асоціацією молекул. Молекули кислот з'єднані попарно за допомогою водневих зв'язків, утворюючи димер:
![]()
Утворенням водневих зв'язків можна пояснити і розчинність карбонових кислот у воді.
Мурашина, оцтова, пропіонова кислоти:
- Безбарвні рідини з різким запахом ;
- Леткі;
- Добре розчинні у воді, 3 – 9% розчин – оцет, 80% - оцтова есенція.
Розчиненню сприяє формування водневого зв’язку між молекулами кислоти і води.
Рідкі
- Масляна кислота та інші ,що мають в молекулі до 9 атомів Карбону, є оліїстими рідинами з неприємним запахом, погано розчиняються у воді.
- Вищі карбонові кислоти (з С10 ) – тверді, без запаху,нерозчинні у воді.
V. Рефлексивно-оцінювальний етап.
 На закінчення - рефлексивний тест.
На закінчення - рефлексивний тест.
1. Дізнався (а) багато нового.
2. Мені це стане в нагоді в житті.
3. Було над чим подумати.
4. На питання, що виникли я отримав (ла) відповідь.
5. Попрацював (а) сумлінно, мета досягнута.
VІ. Етап повідомлення домашнього завдання.
Опрацювати §18, скласти шпаргалку з помилками до теми


про публікацію авторської розробки
Додати розробку
