Робочий зошит 10 клас
 |
Довжик А. А.
Хімія
Робочий зошит
10 клас
___________________________________ ___________________________________ ___________________________________ ___________________________________ ___________________________________ ___________________________________
Київ 2019
Урок 1-2
Повторення початкових понять про органічні речовини
Органічна хімія - _____________________________________________________
Органічні речовини -__________________________________________________ ____________________________________________________________________ Цікаві факти:
Майже всі органічні речовини мають молекулярну будову. Більшість органічних речовин мають запах, погану і хорошу розчинність у воді. До органічних речовин належать не тільки природні речовини,які отримуються із розвитку рослин , або в результаті життєдіяльності тварин, але і багато штучно штучно отриманих в лабораторії речовин. До складу органічних речовин поруч з вуглецем входять деякі хімічні елементи. Це насамперед водень, кисень, азот, сірка, галогени і фосфор. Інші елементи рідко зустрічаються в органічних сполуках. На сьогодні відомо понад 22 мільйони органічних речовин.
Класифікація органічних сполук за якісним складом:
![]() Органічні сполуки
Органічні сполуки
![]()
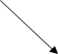
Класифікація органічних сполук за особливостями зв'язку між атомами Карбону:
Органічні сполуки 
Природні органічні речовини:
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Синтетичні органічні речовини:
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Виникнення органічної хімії як науки:
1807 р. - Я. Берцеліус__________________________________________________
____________________________________________________________________
1828 р. - Ф. Велер_____________________________________________________
____________________________________________________________________ 1845 р. - А. Кольбе____________________________________________________
____________________________________________________________________
1845 р. - М. Бертло____________________________________________________
____________________________________________________________________
1861 р. - О. М. Бутлеров________________________________________________
____________________________________________________________________
Насичені органічні сполуки -___________________________________________
____________________________________________________________________
Ненасичені органічні сполуки -_________________________________________
____________________________________________________________________
Ароматичні органічні сполуки -________________________________________
____________________________________________________________________
Гомологи -___________________________________________________________
____________________________________________________________________
Гомологічний ряд -____________________________________________________
____________________________________________________________________
Загальна формула : алканів: ____________________________________________ -алкенів: _____________________; алкінів:________________________________ Гомологічний ряд насичених вуглеводнів:
|
Назва |
Молекулярна формула |
Напівструктурна формула |
|
Метан |
|
|
|
Етан |
|
|
|
Пропан |
|
|
|
Бутан |
|
|
|
Пентан |
|
|
|
Гексан |
|
|
|
Гептан |
|
|
|
Октан |
|
|
|
Нонан |
|
|
|
Декан |
|
|
Структурна формула -_________________________________________________
____________________________________________________________________
Напівструктурна формула -_____________________________________________
____________________________________________________________________
Електронна формула - ________________________________________________
____________________________________________________________________ Вправа 1. Скласти структурну , напівструктурну та електронну формулу для алканів: 1) метану і пропану; 2) пентану і октану.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Насичені вуглеводні (алкани) не вступають у реакції _______________, їм властиві реакції _____________. Насичені і ненасичені вуглеводні мають спільну властивість _________________або___________________________. Продуктами є __________________________.
Унаслідок повного окиснення (горіння) вуглеводнів утворюється вуглекислий газ, вода й виділяється значна кількість теплоти!
Оксигеновмісні органічні речовини -____________________________________
____________________________________________________________________ Приклади:___________________________________________________________ ____________________________________________________________________ Нітрогеновмісні органічні сполуки -_____________________________________ ____________________________________________________________________ Приклади:___________________________________________________________ ____________________________________________________________________
Застосування органічних сполук________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 3-4
Хімічна будова молекул. Ізомерія органічних сполук.
Хімічний зв'язок
Хімічна будова -______________________________________________________ ____________________________________________________________________
Атоми в молекулах органічних речовин сполучені хімічними зв'язками в чітко визначеній послідовності відповідно їх валенстності.
Ізомерія -____________________________________________________________
____________________________________________________________________
____________________________________________________________________
Ізомери -_____________________________________________________________
____________________________________________________________________
____________________________________________________________________
Структурна ізомерія -__________________________________________________
____________________________________________________________________
Скелетна ізомерія -____________________________________________________
____________________________________________________________________ О. М. Бутлеров передбачив існування, крім н-бутану, ще однієї речовини з молекулярною формулою С4Н10- ізобутану, та здійснив її синтез.
 СН3 — СН2 — СН2 — СН3 СН3 — СН — СН3 н-бутан СН3
СН3 — СН2 — СН2 — СН3 СН3 — СН — СН3 н-бутан СН3
ізобутан
Вправа 1. Записати ві можливі ізомери для алканів: а) пентан, б) гептан
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Хімічний зв'язок -_____________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Ковалентний зв'язок -__________________________________________________
____________________________________________________________________ Орбіталь -___________________________________________________________
____________________________________________________________________
Форми електронних орбіталей:__________________________________________
____________________________________________________________________
Утворення ковалентних зв'язків за участю атомів Карбону:__________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Полярність зв'язку -___________________________________________________
____________________________________________________________________
____________________________________________________________________
Йонний зв'язок -______________________________________________________
____________________________________________________________________
Водневий зв'язок -____________________________________________________
____________________________________________________________________ Вправа 2. Наведіть приклади органічних сполук з ковалентним, йонним та водневим зв'язками.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 5
Контрольна робота
Вуглеводні
Урок 6-8
Метан. Насичені вуглеводні (алкани). Ізомерія та номенклатура
Метан -_________________________________________________________
________________________________________________________________
Молекулярна формула:____________________________________________
Електронна і структурна формула:__________________________________
________________________________________________________________
________________________________________________________________ Будова молекули-_________________________________________________
Валентний кут:___________________________________________________ Зв'язки:_________________________________________________________ Фізичні властивості:______________________________________________
________________________________________________________________
________________________________________________________________
Поширення в природі:_____________________________________________ ________________________________________________________________ Добування метану:
а) з алюміній карбіду
б) з метилату натрію
в) з сажи
Насичені вуглеводні -__________________________________________________
____________________________________________________________________
____________________________________________________________________
Загальна формула алканів:_____________________________________________
Найпростіший представник алканів:_____________________________________
Гомологічний ряд -____________________________________________________
____________________________________________________________________
____________________________________________________________________
Гомологи -___________________________________________________________ ____________________________________________________________________ Гомологічний ряд насичених вуглеводнів:
|
Назва |
Молекулярна формула |
Напівструктурна формула |
|
Метан |
|
|
|
Етан |
|
|
|
Пропан |
|
|
|
Бутан |
|
|
|
Пентан |
|
|
|
Гексан |
|
|
|
Гептан |
|
|
|
Октан |
|
|
|
Нонан |
|
|
|
Декан |
|
|
![]() Алканам властива структурна ізомерія, зумовлена різною послідовністю сполучення Карбону в молекулі. Наприклад в бутану є 2 ізомери. Молекула одного з них містить нерозгалужений карбоновий ланцюг, а іншого розгажений. СН3 — СН2 — СН2 — СН3 СН3 — СН — СН3
Алканам властива структурна ізомерія, зумовлена різною послідовністю сполучення Карбону в молекулі. Наприклад в бутану є 2 ізомери. Молекула одного з них містить нерозгалужений карбоновий ланцюг, а іншого розгажений. СН3 — СН2 — СН2 — СН3 СН3 — СН — СН3
н-бутан СН3 2-метилпропан
Складання назв алканів за структурною формулою Правила складання назви алканів:
1.У формулі обирають головний ланцюг, з'ясовують які замісники є у ньому. 2.Нумерують ланцюг (нумерацію починають з того кінця, де ближче стоїть замісник)
3.Визначають назву кожного замісника. Перед назвою кожного замісника через дефіс указують номер атома карбону, з яким сполучений замісник.
4.За наявності кількох однакових замісників зазначають їх кількість, додаючи до назви замісника префікс (ди-, три-, тетра-), а перед ним указують номери атома Карбону.
Замісник -___________________________________________________________
____________________________________________________________________
____________________________________________________________________
Локант -_____________________________________________________________ ____________________________________________________________________
Назви всіх алканів закінчуються суфіксом -ан, а утворені з них одновалентні залишки -ил (-іл).
Приклад:
![]()
![]() Визначити назву ізомеру СН3 — СН — СН2 — СН — СН2 — СН3
Визначити назву ізомеру СН3 — СН — СН2 — СН — СН2 — СН3
С2Н5 СН3
1.Обираємо головний ланцюг:
3
|
СН3 — СН — СН2 — СН — СН2 — СН |
||
|
|
|
|
С2Н5 СН3
2.Нумеруємо:
1 2 3 4 5 6
3
|
СН3 — СН — СН2 — СН — СН2 — СН |
||
|
|
|
|
С2Н5 СН3
3.Визначаємо назви замісників: Вони походять від вуглеводнів (метан — метил, етан — етил, пропан — пропіл: СН3 — метил , С2Н5 — етил , С3Н7 — пропіл, С4Н9 — бутил , С5Н11 — пентил , С6Н13 — гексил)
4.Складаємо назву з замісником і атомом Карбону і назву карбонового ланцюга:
2-етил-4-метилгексан.
Вправа 1. Назвати структурні ізомери :
СН3
![]()
![]()
![]()
![]() а) СН3 — СН2 — СН — СН2 — СН — СН3 ; б) СН3 — С — СН2 — СН — СН3
а) СН3 — СН2 — СН — СН2 — СН — СН3 ; б) СН3 — С — СН2 — СН — СН3
СН3 С2Н5 СН3 С2Н5
____________________________________________________________________ ____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Складання структурної формули алкану за назвою Правила складання структурної формули за назвою:
1.Записують і номерують атоми Карбону, ставлячи між ними одну риску валентності (напрям нумерації не має значення) 2.Записують біля атомів Карбону замісники
3.Дописують у головному ланцюзі атоми Гідрогену в кількості , що забезпечує кожному атому Карбону чотиривалентний стан.
Приклад. Скласти структурну формулу ізомеру: 3-етил-2,5-диметилгептану 1.Записуємо і нумеруємо атоми Карбону:
1 2 3 4 5 6 7
С — С — С — С — С — С — С 2.Записуємо замісники:
1 2 3 4 5 6 7
![]()
![]() С — С — С — С — С — С — С
С — С — С — С — С — С — С
СН3 С2Н5 СН3
3.Дописуємо атоми Гідрогену:
1 2 3 4 5 6 7
![]()
![]()
![]() СН3 — СН— СН — СН2 — СН — СН2 — СН3
СН3 — СН— СН — СН2 — СН — СН2 — СН3
СН3 С2Н5 СН3
Вправа 2. Скласти структурні формули: а) 4-етил-2,2-диметилпентану;
б) 2,5-диетил-4,4-диметилгексану; в) 3-етил-2,4-диметил-6-пропілоктану;
г) 5,7-диетил-2,2,3,6-тетраметилнонану.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ ____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 9 Фізичні та хімічні властивості алканів
Фізичні властивості:___________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Хімічні властивості алканів
Пригадайте:
Реакція заміщення -___________________________________________________ ____________________________________________________________________ Реакція сполучення -__________________________________________________
____________________________________________________________________
Реакція розкладу -____________________________________________________ ____________________________________________________________________ 1. Повне окиснення:
____________________________________________________________________ 2. Неповне окиснення:
____________________________________________________________________
3. Терміний розклад:
1500
![]() а) СН4
а) СН4
1000
б)СН4
в) крекінг
4. Реакція приєднання:________________________________________________
5. Дегідрування:
____________________________________________________________________
6.Ізомеризація:
Реакція ізомеризації -__________________________________________________
____________________________________________________________________
____________________________________________________________________ СН3 — СН2 — СН2 — СН2 — СН3 ![]() 7. Нітрування:
7. Нітрування:
____________________________________________________________________ 8. Галогенування:
1 стадія:_____________________________________________________________
2 стадія:_____________________________________________________________3 стадія:_____________________________________________________________
4 стадія:_____________________________________________________________ Сумарне рівняння галогенування:
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ 9. Взаємодія з водяною парою:
____________________________________________________________________ Задача 1. При спалюванні 5,6 л органічної речовини утворилось 1,8 л вуглекислого газу і 18 г води. Відносна густина пари речовини за вуглекислим газом дорівнює 1. Встановіть молекулярну формулу речовина.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 2. Обчислити об'єм хлорметану, якщо в реакцію з метаном вступає хлор кількістю речовини 4 моль.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Вправа 1. Здійснити перетворення: С → СН4→СН3Br→C2H6→C2H5CI →C4H10
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 10-11
Алкени. Структурна ізомерія та номенклатура
Алкени -____________________________________________________________
____________________________________________________________________
____________________________________________________________________ Загальна формула алкенів -_____________________________________________ Перший представник алкенів -__________________________________________ Структурна і електрона формула етину:
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
Ізомерія
Алкенам як і алканам властива просторова ізомерія. Якщо в алкану з молекулярною формулою С4Н10 існує два ізомери, то в алкену з такою самою кількістю атомів Карбону їх три.
СН2 — СН — СН2— СН3 СН2 — СН — СН — СН3
бут-1-ен бут-2-ен
![]() СН2 — СН — СН3
СН2 — СН — СН3
СН3
2-метилпроп-1-ен
Вправа 1. Скласти структурні формули ізомерів пентену. Назвати їх.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Загальні правила складання назв алкенів:
1.Обирають головний ланцюг — найдовший карбоновий ланцюг з подвійним зв'язком.
2.Нумерацію починають де ближче стоїть подвійний зв'язок.
3.Назви алкенів утворюються від назв алканівз такою самою кількостю атомів, але змінюючи суфікс -ан на -ен.
4.Перед суфіксом -ен записують локант подвійного зв'язку, виділяючи його з обох боків дефісами.
5.Повну назву складають у такій самій послідовності що й для алканів, за винятком того що перед суфіксом -ен додається локант подвійного зв'язку.
Приклад:
![]()
![]()
![]() Скласти назву ізомеру: СН2 — СН — СН2 — СН — С
Скласти назву ізомеру: СН2 — СН — СН2 — СН — С — СН3
СН3 СН3 С2Н5
1.Обираємо головний ланцюг з подвійним зв'язком:
![]() СН3— СН — СН2 — СН — С
СН3— СН — СН2 — СН — С — СН3
СН3 СН3 С2Н5
2.Нумеруємо головний ланцюг, визначають локант подвійного зв'язку:
6 5 4 3 2 1
![]() СН3— СН — СН2 — СН — С
СН3— СН — СН2 — СН — С — СН3
СН3 СН3 С2Н5
За нумерацією бачимо що це гекс-1-ен.
3.З'ясовуємо які є замісники у карбоновому ланцюзі і складаємо назву замісників: 2-етил-3,5-диметил
4.Після цього складаємо повну назву: 2-етил-3,5-диметилгекс-1-ен Вправа 2. Скласти назви ізомерів: а)
СН3 — СН2 — СН — СН2 — С — СН — СН3
![]()
![]()
СН3 С2Н5
б)
СН3 — СН — СН — С — СН2 — СН3
![]()
![]()
С3Н7 СН3
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Вправа 3. Скласти структурну формулу : а) 4-етил-3,3-диметилпент-1ену; б) 2,2-диметилгекс-3-ену; в) 5-етил-3,4,7,7-тетраметилокт-1-ену.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 12 Хімічні властивості алкенів
Пригадайте:
Полімеризація -_______________________________________________________
____________________________________________________________________
____________________________________________________________________
Мономер -___________________________________________________________
____________________________________________________________________
Полімер -____________________________________________________________
____________________________________________________________________
Фізичні властивості:___________________________________________________
____________________________________________________________________
____________________________________________________________________ ____________________________________________________________________
1.Окиснення
а) повне окиснення:
____________________________________________________________________ б) неповне окиснення:
____________________________________________________________________ 2. Галогенування:
____________________________________________________________________
____________________________________________________________________ 3. Гідрування (приєднання водню):
____________________________________________________________________ 4. Приєднання галогеноводнів:
____________________________________________________________________
____________________________________________________________________ 5. Заміщення:
____________________________________________________________________ 6. Гідратація (приєднання води):
____________________________________________________________________ 7. Полімеризація:
____________________________________________________________________
____________________________________________________________________ Задача 1.Алкен масою 2,8 г приєднав 2,24 л хлору. Знайдіть молекулярну формулу сполуки.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 2.Обчислити об'єм етану, що утвориться в результаті реакції гідрування етену, кількістю речовини 2 моль.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Вправа 1. Здійснити перетворення: C2H6 →C2H4→ C2H4CI2
↓
C2H5OH
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 13-14
Алкіни. Номенклатура. Хімічні властивості
Алкіни -_____________________________________________________________
____________________________________________________________________
____________________________________________________________________
Загальна формула алкінів:______________________________________________ Перший представник алкінів:___________________________________________ Скласти електрону і структурну формулу етину:
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Фізичні властивості:___________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ За ситематичною номенклатурою назви алкінів утворюються від назв алканів з такою самою кількістю атомів Карбону в молекулі, змінюючи в назві головного ланцюга суфікс -ан на -ин(-ін). Наприклад етан — етин , пропан — пропін , бутан — бутин , пентан — пентин. Решта правил номенклатури такі самі, як для алкенів.
Вправа 1. Скласти структурні формули: а) пент-1-ин; б) 3-метилбут-1-ин; в)2-етил-4,4,6-триметилгепт-1-ин; г) 4,5-диетил-2-метилгекс-1-ин.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Хімічні властивості:
1.Окиснення:
а) окиснення розчином КМnО4
____________________________________________________________________ ____________________________________________________________________ б) повне окиснення
____________________________________________________________________ ____________________________________________________________________
2. Гідрування
____________________________________________________________________
3.Галогенування
____________________________________________________________________ ____________________________________________________________________
4.Заміщення
____________________________________________________________________
5.Приєднання гідроген галогенідів
____________________________________________________________________ ____________________________________________________________________
6. Гідратація
____________________________________________________________________
____________________________________________________________________ Задача 1. Яка маса кальцій карбіду, що прореагував з водою, якщо в результаті виділився ацетилен об'ємом 5,6 л.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Задача 2. Визначте масові частки речовин у суміші, що уворились в результаті пропіну об'ємом 10 л і хлороводню об'ємом 14 л. Об'єми газів виміряні за однакових умов.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Вправа 1. Здійснити перетворення: C2H6 → C2H2→ C2H4 → C2H5Br
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 15
Ароматичні вуглеводні. Бензен
Ароматичні вуглеводні -________________________________________________
____________________________________________________________________
____________________________________________________________________ Найпростіший представник ароматичних вуглеводнів:______________________ Структурна формула бензену:
Історія відкриття бензену:______________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Фізичні властивості:
____________________________________________________________________
____________________________________________________________________ Хімічні властивості:
1.Окиснення:
2. Гідрування
____________________________________________________________________
____________________________________________________________________
3. Приєднання галогенів
____________________________________________________________________
____________________________________________________________________
4. Приєднання гідроген галогенів
____________________________________________________________________
____________________________________________________________________ Вправа 1. Написати структурні формули таких сполук: бензен, нафтален, антрацен, дифеніл
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 1. Який об'єм водню за нормальних умов може приєднати бензен кількістю речовини 0,2 моль?
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 2. Яку масу бромбензолу можна добути із суміші 64 г брому і 15,6 г бензолу за наявності каталізатора FeBr3?
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Вправа 2. Здійснити перетворення С → СН4→ СН3Br→ C2H6→ C2H2 → C6H6 ____________________________________________________________________
Урок 16 Добування вуглеводнів
1.Добування метану а) з алюміній карбіду
____________________________________________________________________ б)З натрій ацетату і гідроксиду натрію
____________________________________________________________________ в) З сажи і водню
____________________________________________________________________ г) Гідрування алкенів
____________________________________________________________________ д) Гідрування алкінів
____________________________________________________________________ е) Крекінг алканів
____________________________________________________________________ 2. Добування етену
а) Крекінг алканів
____________________________________________________________________ б) Дегідрування алканів
____________________________________________________________________ в) Дегідратація спиртів
____________________________________________________________________
3. Добування етину
а)Дегідрування метану
____________________________________________________________________ б)Гідроліз кальцій ацетаніліду СаС2
____________________________________________________________________ в)Дегідрування етану
____________________________________________________________________ г) Дегідрування етену
____________________________________________________________________
4. Добування бензену
а)Дегідрування і циклізація алканів у присутності каталізатора
б)Дегідрування циклогексану
____________________________________________________________________ в) Тримеризація етину
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 17 Контрольна робота
Оксигеновмісні органічні сполуки
Урок 18 - 19
Спирти. Номенклатура. Хімічні властивості
Спирти -_____________________________________________________________
____________________________________________________________________
____________________________________________________________________ Загальна формула спиртів:______________________________________________ Класифікація спиртів:
1. За кількістю гідроксильних груп:
а)___________________________________________________________________
б)___________________________________________________________________
в)___________________________________________________________________ 2. Залежно від наявності кратних зв'язків:
а)___________________________________________________________________
б)___________________________________________________________________
в)___________________________________________________________________ 3. Залежно від положення гідроксильної групи в карбоновому ланцюзі:
а)___________________________________________________________________
б)___________________________________________________________________
в)___________________________________________________________________ Фізичні властивості:___________________________________________________
____________________________________________________________________
____________________________________________________________________ Правила складання назви :
1.Обирають головний найдовший карбоновий ланцюг із гідроксильною групою
2.Нумерують головний ланцюг
3.Визнають назви замісників
4.Складають назву спирту
Систематична назва спирту складається з назви відповідного алкану і суфікса -ол : метан — метанол, етан — етанол.
Вправа 1. Скласти структурні формули ізомерів: а) 2-метилбутан-3-ол; б) 2,4-диметилгексан-3-ол; в) 3,3-диетил-4,6-диметилгептан-2-ол.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Вправа 2. Скласти назву ізомеру : СН3
а) б)
![]()
![]()
![]()
![]()
![]() СН3 — СН — СН — СН2 — СН3 СН3 — С — СН — СН2 — СН — СН3
СН3 — СН — СН — СН2 — СН3 СН3 — С — СН — СН2 — СН — СН3
СН3 ОН СН3 ОН С2Н5
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 20 - 21
Насичені одноатомні спирти. Фізичні та хімічні властивості
Одноатомні спирти -___________________________________________________ ____________________________________________________________________
Фізичні властивості:___________________________________________________
____________________________________________________________________ Загальна формула насичених одноатомних спиртів:________________________ Гомологічний ряд одноатомних спиртів:
метанол — СН3ОН гексанол — С6Н13ОН етанол — С2Н5ОН гептанол — С7Н15ОН пропанол — С3Н7ОН октанол — С8Н17ОН бутанол — С4Н9ОН нонанол — С9Н19ОН пентанол — С5Н11ОН деканол — С10Н21ОН
Вправа 1. Скласти електронну і структурну формулу метанолу і етанолу
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Хімічні властивості:
1.Окиснення:
а) Повне окиснення
____________________________________________________________________ б) Часкове окиснення
____________________________________________________________________
2.Дегідратація
____________________________________________________________________
____________________________________________________________________
3. Взаємодія з активними металами
____________________________________________________________________
____________________________________________________________________
4. Взаємодія з гідрогенгалогенідами
____________________________________________________________________
____________________________________________________________________
5. Взаємодія з кислотами
____________________________________________________________________
____________________________________________________________________ Добування етанолу і метанолу:
1.Гідратація етену
____________________________________________________________________
2. Спиртове бродіння глюкози
3. Із синтез-газу
4. Відновлення альдегідів і кислот
Фізіологічна дія метанолу і етанолу:
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Застосування метанолу і етанолу:
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 1. Під час взаємодії етанолу масою 13,8 г з CuO масою 28 г отримали альдегід, маса якого становила 9,24 г. Визначити вихід продукту.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 2. Етанол масою 230 г піддали окисненню в присутності каталізатора. Утворилася етанова кислота кількістю речовини 4 моль. Обчисліть масову частку домішок реагенту.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Урок 22
Багатоатомні спирти. Етиленгліколь і гліцерин
Двохатомні спирти -___________________________________________________
____________________________________________________________________
Багатоатомні спирти - _________________________________________________
____________________________________________________________________
Фізичні властивості етиленгліколю і гліцеролу:____________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Вправа 1. Записати електрону і структурну формулу етиленгліколю і гліцерину
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Хімічні властивості:
1.Окиснення
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
2. Приєднання гідроген галогенідів
____________________________________________________________________
____________________________________________________________________
3.Реакція з активними металами
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
4.Реакція з Сu(ОН)2
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ ____________________________________________________________________ Добування :
1.етиленгліколю
____________________________________________________________________
2. гліцеролу
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Застосування етиленгліколю і гліцеролу:
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Задача 1. Напишіть рівняння взаємодії свіжоосадженого Сu(ОН)2 з розчином 1,2-етандіолу. Обчисліть масу етандіолу що прореагує з Сu(ОН)2 масою 58,8 г.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 2. Трохатомний спирт масою 300 г прореагував з металічним натрієм, унаслідок чого утворилася сіль кількістю речовини 2,5 моль. Визначте формулу спирту. Зобразіть його структурну формулу.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 3. Обчислити об'єм водню, що виділився при взаємодії натрію з гліцерином масою 184 г.
____________________________________________________________________
Урок 23
Фенол. Фізичні та хімічні властивості
Фенол -______________________________________________________________
____________________________________________________________________
____________________________________________________________________
Молекулярна формула:________________________________________________
Структурна формула:__________________________________________________
____________________________________________________________________
____________________________________________________________________
Фізичні властивоті:____________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Хімічні властивості:
1.Взаємодія з лужними металами
____________________________________________________________________
____________________________________________________________________
2. Взаємодія з лугами
____________________________________________________________________
3.Взаємодія з бромною водою
____________________________________________________________________ Добування фенолу:
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Фізіологічна дія:______________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Застосування:________________________________________________________ Задача 1. Фенол масою 9,2 г взаємодіє з натрієм. Який об'єм при цьому виділиться?
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 2. На розчин фенолу масою 100 г із масовою часткою 0,47 подіяли розчином гідроксидом натрію. Обчисліть масу солі що утворилася.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 24-25 Альдегіди
Альдегіди -__________________________________________________________
____________________________________________________________________
____________________________________________________________________
Загальна формула:____________________________________________________
____________________________________________________________________
Карбонільна група:___________________________________________________
Альдегідна група:_____________________________________________________
Фізичні властивості:___________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Хімічні властивості:
1.Відновленн етаналю воднем
2. Реакції часткового окиснення
а) Окиснення киснем повітря
____________________________________________________________________ ____________________________________________________________________ б) Окиснення амоніачним розчином Ag2O (реакція срібного дзеркала) ____________________________________________________________________ ____________________________________________________________________ в) Окиснення Cu(OH)2
____________________________________________________________________
____________________________________________________________________
Добування етаналю
1.Гідратація етину за наявності солей Меркурію
____________________________________________________________________
____________________________________________________________________
2.Окиснення етанолу
____________________________________________________________________
____________________________________________________________________
|
Назва альдегіду |
Формула |
|
Метаналь |
|
|
Етаналь |
|
|
Пропаналь |
|
|
Бутаналь |
|
|
Пентаналь |
|
Щоб назвати альдегід:
1.Обирають найдовший головний карбоновий ланцюг до складу якого входить альдегідна група.
2.Локант1 присвоюють атому Карбону альдегідної групи 3.З'ясовують які є замісники та їх локанти
4.Називають сполуку.
Вправа 1. Назвати сполуки
а) СН3 О б) О
![]()
![]() СН3 — С — СН — С СН3 — СН — СН2 — СН — С
СН3 — С — СН — С СН3 — СН — СН2 — СН — С ![]()
![]()
![]() СН3 С2Н5 Н С2Н5 СН3 Н в) С2Н5 О
СН3 С2Н5 Н С2Н5 СН3 Н в) С2Н5 О
![]() СН3 — СН2 — С — СН2 — СН — С
СН3 — СН2 — С — СН2 — СН — С ![]()
![]() С2Н5 СН3 Н
С2Н5 СН3 Н
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Вправа 2. Скласти структурні формули: а) 2,2-диметилпентаналю; б)5-етил-3,3диметилгексаналю; в) 2,4-диетил-5,5,7-триметилоктаналю.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 1.В результаті окиснення технічного ацетальдегіду надлишком аміачного розчину Ag2O утворилось 2,16 г срібла. Визначити масову частку ацетальдегіду в технічному препараті?
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 2. Яка маса срібла виділиться внаслідок окиснення оцтового альдегіду масою 22 г потрібною кількістю аміачного розчину Ag2O ?
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Вправа 3. Здійснити перетворення О
СН4→ СН3СІ→ С2Н6→ С2Н4→ С2Н5ОН → СН3 — С
![]() Н ____________________________________________________________________
Н ____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 26-28
Карбонові кислоти
Карбонові кислоти -___________________________________________________
____________________________________________________________________
____________________________________________________________________
Загальна формула карбонових кислот:____________________________________ Карбоксильна група:___________________________________________________ Класифікація:
1.За кількістю карбоксильних груп
а)___________________________________________________________________
б)___________________________________________________________________
2.За будовою вуглеводневого залишку
а)___________________________________________________________________
б)___________________________________________________________________
в)___________________________________________________________________
3.За кількістю атомів Карбону в молекулі кислоти
а)___________________________________________________________________
б)___________________________________________________________________ Загальна формула насичених одноосновних карбонових кислот:______________
____________________________________________________________________ Приклади:___________________________________________________________ ____________________________________________________________________ Заповнити таблицю
|
Назва алкану |
Формула кислоти |
Систематична назва кислоти |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вищі карбонові кислоти -______________________________________________ ____________________________________________________________________ Класифікація :
1.___________________________________________________________________
2.___________________________________________________________________
Приклади:___________________________________________________________ ____________________________________________________________________
____________________________________________________________________ Вправа 1. Написати структурну формулу бутанової кислоти і 2-метилпропанової кислоти.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Фізичні властивості етанової кислоти :___________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Хімічні властивості етанової кислоти:
1.Електролітична дисоціація
|
|
|
|
____________________________________________________________________ 2.Реакції з утворенням солей
а) Взаємодія з металами
____________________________________________________________________ б) Взаємодія з основними і амфотерними оксидами
____________________________________________________________________ ____________________________________________________________________ в) Взаємодія з основами і амфотерними гідроксидами
____________________________________________________________________ ____________________________________________________________________ г) Взаємодія з солями слабких кислот
____________________________________________________________________
3. Реакція зі спиртами
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Реакція естерифікації -_________________________________________________
____________________________________________________________________
____________________________________________________________________
Лабораторний дослід № 1
Виявлення органічних кислот в харчових продуктах
Реактиви і обладнання : хімічні стакани, пробірки, штатив, універсальний індикаторний папір, розчини метил оранжевого і лакмусу, харчові продукти. 1.Проведіть дослідження. Для цього на кожен із зразків досліджуваних продуктів крапніть по черзі індикатори.
2.Запишіть результати у таблицю. 3.Зробіть висновок
|
Продукти |
Забарвлення лакмусу |
Забарвлення метил оранжевого |
Забарвлення універсального паперу |
Висновок |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Висновок:____________________________________________________________
____________________________________________________________________
____________________________________________________________________
Добування оцтової кислоти
1.Окиснення етанолу
____________________________________________________________________ 2. Окиснення етаналю
____________________________________________________________________ Задача 1. Яку масу оцтової кислоти і води треба взяти для приготування розчину масою 50 г з масовою часткою розчиненої речовини 9%?
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 2. Магній масою 5 г провзаємодіяв з оцтовою кислотою. Який об'єм газу при цьму виділився?
____________________________________________________________________
____________________________________________________________________ ____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 3. Масові елементів у молекулі одноосновної карбонової кислоти становлять: 26,1% С, 4,35% Н, 69,55% О. Яка назва цієї кислоти?
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 29-30
Естери. Гідроліз естерів. Жири
Естери -_____________________________________________________________
____________________________________________________________________
____________________________________________________________________
Загальна формула естерів:______________________________________________
____________________________________________________________________
Фізичні властивості:___________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Реакція гідролізу -_____________________________________________________
____________________________________________________________________
____________________________________________________________________
Гідроліз естеру
____________________________________________________________________
____________________________________________________________________
Жири -______________________________________________________________
____________________________________________________________________
____________________________________________________________________
Загальна формула жирів:_______________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Класифікація:
1.___________________________________________________________________
2.___________________________________________________________________
Фізичні властивості:___________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Хімічні властивості 1. Гідроліз жирів
а) кислотний
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ ____________________________________________________________________ б) лужний
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Мила -______________________________________________________________
____________________________________________________________________
____________________________________________________________________
Тверде мило:_________________________________________________________
____________________________________________________________________
Рідке мило:__________________________________________________________
____________________________________________________________________
2. Гідрування жирів
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Застосування жирів:___________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Біологічна роль жирів:_________________________________________________ ____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Жири в природі:______________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 1. Під час нагівання метанолу масою 2,4 г і етанової кислоти масою 3,6 г отримали естер метилетаонат (метилацетат) масою 3,7 г.Визначте вихід естеру. ____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Вправа 1. Здійснити такі перетворення
О
СН4→ С2Н2 → С2Н4 → СН3СООН→ СН3 — С
![]() О — С2Н5
О — С2Н5
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 2. Яку масу тристеарину необхідно, щоб добути гліцерин масою 9,2 г?
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 3. На гідрування триолеїну витратили водень об'ємом 33,6 л. Яку масу жиру було взято?
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Вправа 2. Як добувають маргарин?
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 4. Розрахуйте масу гліцеролу. Який можна добути з 1 кг трипльмітину.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 31-32
Вуглеводи. Глюкоза
Вуглеводи -__________________________________________________________
____________________________________________________________________
____________________________________________________________________ Класифікація:
Вуглеводи


Моносахариди -______________________________________________________ Дисахариди -_________________________________________________________
____________________________________________________________________
____________________________________________________________________ Полісахариди -_______________________________________________________
____________________________________________________________________
____________________________________________________________________
Поширення в природі:_________________________________________________
____________________________________________________________________
____________________________________________________________________
Глюкоза
Молекулярна формула глюкози:_________________________________________ Структурні формула глюкози:
а) альдегідна форма-___________________________________________________
____________________________________________________________________
б) альфа- циклічна форма-______________________________________________
____________________________________________________________________
в) бета- циклічна форма-_______________________________________________ ____________________________________________________________________ Фізичні властивості глюкози:___________________________________________
____________________________________________________________________
____________________________________________________________________
Поширення в природі:_________________________________________________
____________________________________________________________________
____________________________________________________________________ Хімічні властивості глюкози:
1. Реакції за участю гідроксильних груп (на прикладі взаємодії з Cu(OH)2)
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ 2. Реакції за участю альдегідної групи
а) Відновлення воднем
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ ____________________________________________________________________ б)Часткове відновлення Cu(ОН)2
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
в) часкове окиснення амоніачним розчином Ag2O (реакція срібного дзеркала) ____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Лабораторний дослід №2
Окиснення глюкози свіжоосадженим Cu(ОН)2
Реагенти і обладнання: пробірки, штатив, спиртівка, тримач для пробірок, розчини CuSO4, NaOH і глюкози, гаряча вода, хімічний стакан.
1.У пробірку налийте 2 мл CuSO4 і 2 мл NaOH.
Рівняння реакції:______________________________________________________
Спостереження: ______________________________________________________ 2.До осаду Cu(ОН)2 налийте 2 мл глюкози й перемішайте вміст пробірки струшуванням.
Рівняння реакції:______________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Спостереження:______________________________________________________
____________________________________________________________________ 3. Пробірку з результатом злегка нагріти , зануривши її в стакан з гарячою водою.
Спостереження:______________________________________________________
____________________________________________________________________
Висновок:____________________________________________________________
____________________________________________________________________
____________________________________________________________________
3. Бродіння глюкози
а) спиртове бродіння
____________________________________________________________________ ____________________________________________________________________ б) молочнокисле бродіння
____________________________________________________________________
____________________________________________________________________ Задача 1. Глюкозу масою 1260 кг, піддали спиртовому бродінню. Яка маса етанолу при цьому утворилась?
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 2. Який об'єм вуглекислого газу виділиться при спртовому бродінні 225 г глюкози?
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Вправа 1. Дописати рівняння реакцій ферменти а) С6Н12О6 →
б) С6Н12О6 + Ag2O →
в) С6Н12О6 + Cu(OH)2 →
Урок 33
Дисахариди. Сахароза
Дисахариди -_________________________________________________________
____________________________________________________________________
____________________________________________________________________
Сахароза -___________________________________________________________
____________________________________________________________________
Молекулярна формула сахарози:________________________________________
Фізичні властивості:___________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Поширення в природі:_________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Хімічні властивості
1.Гідроліз
____________________________________________________________________
____________________________________________________________________ 2. Взаємодія з Cu(ОН)2 ____________________________________________________________________
____________________________________________________________________
3. Взаємодія сахарози з Cа(ОН)2
____________________________________________________________________ Загальна схема виробництва цукру:
Застосування сахарози:________________________________________________ ____________________________________________________________________
____________________________________________________________________ Задача 1. Яка маса гюкози утвориться під час гідролізу сахарози масою 34,2 г ?
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 2. Обчисліть кількість молекул сахарози в 68,4 г сахарози.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 34
Полісахариди. Крохмаль, целюлоза
Пригадайте:
Полімери -______________________________________________________
________________________________________________________________
Полімеризація -__________________________________________________
________________________________________________________________ Полісахариди -_______________________________________________________
____________________________________________________________________
____________________________________________________________________
Крохмаль і целюлоза — природні полімери
Найважливішими полісахаридами є:_____________________________________
|
Характеристики |
Крохмаль |
Целюлоза |
|
Молекулярна формула |
|
|
|
Будова молекул(форма) |
|
|
|
Склад молекули |
|
|
|
Молекулярна маса |
|
|
|
Фізичні властивості |
|
|
|
Поширення в природі |
|
|
|
Застосування |
|
|
Молекулярне рівняння утворення полісахаридів:
____________________________________________________________________
____________________________________________________________________ Хімічні властивості крохмалю:
![]()
![]()
![]() 1.Гідроліз крохмалю: крохмаль
1.Гідроліз крохмалю: крохмаль декстрини мальтоза глюкоза
____________________________________________________________________
____________________________________________________________________
2. Реакція з йодом
____________________________________________________________________
____________________________________________________________________
3. Термічний розклад
____________________________________________________________________ ____________________________________________________________________ Хімічні властивості целюлози :
1. Гідроліз: __________________________________________________________
2. Окиснення:________________________________________________________Задача 1. Який об'єм кисню виділився під час фотосинтезу якщо утворилося 8 моль крохмалю?
____________________________________________________________________
____________________________________________________________________ ____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ ____________________________________________________________________ Задача 2
Розрахуйте масу розчину нітратної кислоти з масовою часткою 60% неохідно для добування 0,5 кг тринітроцелюлози.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 35
Практична робота № 1
Розв'язування експериментальних задач
Пригадйте правила техніки безпеки під час роботи з кислотами та лабораторним посудом і приладдям, суворо дотримуйтесь їх!
Завдання 1. Дослідним шляхом розпізнати а) глюкозу і крохмаль; б) гліцерол і сахарозу. Виконання дій та спостереження записати у таблицю. Написати рівняння відповідних реакцій.
Завдання 2. У трьох пробірках містяться розчини гліцеролу, етанової кислоти і етаналю. Дослідним шляхом виявіть наявність цих речовин. Виконання дій та спостереження записати у таблицю. Написати рівняння відповідних реакцій.
|
Виконання дій |
Спостереження |
Рівняння реакцій |
Висновки |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Урок 36 Контрольна робота
Нітрогеновмісні сполуки
Урок 37-38
Аміни
Аміни -______________________________________________________________
____________________________________________________________________
____________________________________________________________________ Класифікація:
1.Залежно від природи вуглеводневих замісників:
а)___________________________________________________________________
б)___________________________________________________________________ Приклади:
____________________________________________________________________
____________________________________________________________________ 2.За кількістю вуглеводневих залишків:
а)___________________________________________________________________
б)___________________________________________________________________
в)___________________________________________________________________ Приклади:
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Правила назви амінів:
1.Обирають головний найдовший карбоновий ланцюг, один із атомів Карбону сполучений з аміногрупою.
2.Нумерують головний ланцюг за принципом найменшого локанта аміногруп.
3.З'ясовують назви замісників.
4.Складають назву аміну.
Вправа 1. Скласти назву сполуки:
а) СН3
![]() СН3 — СН2 — С — СН2 — СН — СН2 — СН2 – NH2
СН3 — СН2 — С — СН2 — СН — СН2 — СН2 – NH2
![]() СН3 C2Н5
СН3 C2Н5
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Вправа 2. Скласти структурні формули: а) 2,2-диетил-3-метилпентан-1-аміну; б) 4,4-диметилгексан-1-аміну; в) 3-етил-5,5-диметилгептан-2-аміну.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Застосування:________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Фізіологічна дія:______________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 1.Обчисліть масу диметиламіну, який може прореагувати із хлороводнем об'ємом 3,36 л.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 2. Яку масу аміну одержали в результаті взаємодії амоніаку об'ємом 4,48 л з брометаном масою 10,9 г?
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 39 Анілін
Молекулярна формула:_________________________________________________
Структурна формула:__________________________________________________
____________________________________________________________________
Фізичні властивості:___________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Хімічні властивості:
1.Взаємодія з кислотами
____________________________________________________________________
____________________________________________________________________
2. Взаємодія з бромною водою
____________________________________________________________________
____________________________________________________________________ Добування
1.Відновлення нітробензену
____________________________________________________________________
____________________________________________________________________ Застосування:________________________________________________________
____________________________________________________________________ ____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 1. Зразок нітробензену масою 85 г, в якому масова частка домішок 7%, відновили до аніліну. Вихід реакції дорівнює 85%. Обчисліть масу аніліну що утворився.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 2. Обчисліть масу аніліну , який утвориться з нітробензолу масою 503 г та водню масою 24 г.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 40-41
Амінокислоти. Пептиди
Амінокислоти -_______________________________________________________
____________________________________________________________________
____________________________________________________________________ Загальна формула:
Класифікація амінокислот:
1) За числом аміногруп:
а)___________________________________________________________________
б)___________________________________________________________________ 2) За числом карбоксильних груп:
а)___________________________________________________________________
б)___________________________________________________________________ 3) За положенням аміногрупи:
а)____________________________ в)_____________________________
б)____________________________ г)_____________________________ Біполярний йон -______________________________________________________ Фізичні властивості:___________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Поширення в природі:_________________________________________________
____________________________________________________________________
____________________________________________________________________ Заповнити таблицю:
|
Кислота |
Амінокислота |
Напівструктурна формула |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Правила складання назви амінокислот
1.Обирають головний ланцюг, нумерацію починаємо з атома Карбону карбоксильної групи.
2.У назві перед префіксом “аміно” записують локант.
3.Складають назву амінокислоти.
Вправа 1. Скласти структурні формули кислот :а) 3-аміно-2,3-диметилбутанової б) 2-аміно-3,3,4-триметилпентанової
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Хімічні властивості аміноетанової кислоти:
1. Взаємодія з кислотами
____________________________________________________________________
____________________________________________________________________
2. Взаємодія з лугами
____________________________________________________________________
____________________________________________________________________
3. Взаємодія амінокислот між собою
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Поліконденсація -_____________________________________________________
____________________________________________________________________
Пептиди -____________________________________________________________
____________________________________________________________________ Пептидний зв'язок -___________________________________________________ ____________________________________________________________________
Пептидна група -_____________________________________________________ ____________________________________________________________________ Утворення пептиду:
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Вправа 2. Написати структурні формули а)гліцину і аланіну, б)гліцину і валіну і зобразити схему утворення дипептиду
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Вправа 2. Написати структурні формули аланіну, лейцину і валіну і зобразити утворення трипептиду
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Задача 1. Аміноетанова кислота, масою 67,5 г, вступила в реакцію з натрій гідроксидом. Яка маса солі натрій аміноацетату утворилась?
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ ____________________________________________________________________
Урок 42-43
Білки. Біологічна роль білків і амінокислот
Білки -______________________________________________________________
____________________________________________________________________
____________________________________________________________________
|
Характеристики |
Особливості білкових молекул |
|
Молекулярна маса |
|
|
Елементний склад |
|
|
Фізичні властивості |
|
|
Класифікація |
|
|
а) за хімічним складом |
|
|
б) за фізіологічними функціями |
|
|
Номенклатура |
|
|
Знаходження в природі |
|
Будова молекули білка:
Первинна структура -__________________________________________________
____________________________________________________________________
____________________________________________________________________
Вторинна структура -__________________________________________________
____________________________________________________________________
____________________________________________________________________
Третинна структура -__________________________________________________
____________________________________________________________________
____________________________________________________________________
Четвертинна структура -_______________________________________________ ____________________________________________________________________ Хімічні властивості:
1.Гідроліз білків
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
2.Денатурація
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
3.Кольорові реакції
а) біуретова реакція -__________________________________________________
____________________________________________________________________ б) ксантопротеїнова реакція -___________________________________________ ____________________________________________________________________
Лабораторний дослід № 3
Біуретова реакція
Обладнання і реактиви: пробірки, розчини курячого яйця, лугу і CuSO4.
Завдання 1. Розчинніть курячий білок у воді.
Завдання 2. До розчину білка 2 мл долийте 2 мл лугу. Додайте кілька крапель розчину CuSO4 .
Спостереження і висновки запишіть у таблицю:
|
Що робили? |
Спостереження |
Висновок |
|
|
|
|
|
|
|
|
Висновок:____________________________________________________________
____________________________________________________________________
____________________________________________________________________
Лабораторний дослід № 4
Ксантопротеїнова реакція
Обладнання і реактиви: пробірки, розчини курячого яйця, концентрованої нітратної кислоти.
Завдання 1. Розчинніть курячий білок у воді.
Завдання 2. До розчину білка 2 мл долийте 1 мл концентрованої нітратної кислоти.
Спостереження і висновки запишіть у таблицю:
|
Що робили? |
Спостереження |
Висновок |
|
|
|
|
|
|
|
|
Висновок:____________________________________________________________
____________________________________________________________________
____________________________________________________________________
Ферменти -___________________________________________________________
____________________________________________________________________
Біологічна роль білків:_________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________ Біологічна роль амінокислот:___________________________________________ ____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 44 Контрольна робота
Синтетичні високомолекулярні сполуки і матеріали
Урок 45-46
Синтетичні високомолекулярні сполуки
Пригадайте:
Полімер -____________________________________________________________
____________________________________________________________________
Мономер -___________________________________________________________
____________________________________________________________________
Структурна ланка -____________________________________________________
____________________________________________________________________
Ступінь полімеризації -________________________________________________ ____________________________________________________________________ Класифікація полімерів:
1. За походженням
а)___________________________________________________________________
б)___________________________________________________________________
2. За елементним складом
а)___________________________________________________________________
б)___________________________________________________________________
в)___________________________________________________________________
3. За формою молекули
а)___________________________________________________________________
б)___________________________________________________________________
в)___________________________________________________________________ Природні полімери -___________________________________________________
____________________________________________________________________
Синтетичні полімери -_________________________________________________
____________________________________________________________________
Лінійні полімери -_____________________________________________________
____________________________________________________________________
Розгалужені полімери -________________________________________________
____________________________________________________________________
Сітчасті полімери -____________________________________________________
____________________________________________________________________
Органічні полімери -__________________________________________________
____________________________________________________________________
Неорганічні полімери -________________________________________________
____________________________________________________________________
Елементорганічні полімери -___________________________________________
____________________________________________________________________
Термопластичність -___________________________________________________
____________________________________________________________________
____________________________________________________________________
Термопластичні полімери -_____________________________________________
____________________________________________________________________
____________________________________________________________________ Термореактивні полімери -_____________________________________________ ____________________________________________________________________
____________________________________________________________________
Реакція полімеризації -________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Вправа1. Навести схему утворення поліетилену, поліпропілену, полістирену, полівінілхлориду.
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Реакція поліконденсації -_______________________________________________
____________________________________________________________________
____________________________________________________________________
Вправа 2. Навести схему поліконденсації двохатомного спирту етиленгліколю
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 47
Пластмаси. Каучуки. Гума
Матеріали -__________________________________________________________
____________________________________________________________________
Пластмаси -__________________________________________________________
____________________________________________________________________ Основою пластмас є:__________________________________________________ Найпоширеніші пластмаси:
Поліетилен -_________________________________________________________
____________________________________________________________________
Поліпропілен -_______________________________________________________
____________________________________________________________________
Полівінілхлорид -_____________________________________________________
____________________________________________________________________
Полістирен -_________________________________________________________
____________________________________________________________________
Фенолоформальдегідні смоли -__________________________________________
____________________________________________________________________
Каучуки -____________________________________________________________
____________________________________________________________________
Характерна властивість каучуків:________________________________________
____________________________________________________________________ Природні каучуки -____________________________________________________
____________________________________________________________________
Синтетичні каучуки -__________________________________________________ ____________________________________________________________________ Види каучуків:
а)___________________________________________________________________
б)___________________________________________________________________
в)___________________________________________________________________ Загальна схема утворення каучуків:
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Вправа 1. Напишіть схему реакції полімеризації бута-1,3-дієну
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 48
Волокна. Природні та хімічні волокна
Волокна -____________________________________________________________
____________________________________________________________________
____________________________________________________________________ Класифікація:
Волокна
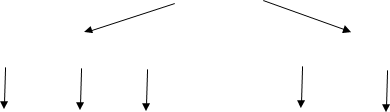
Природні волокна -____________________________________________________ ____________________________________________________________________
Синтетичні волокна -__________________________________________________
____________________________________________________________________
Лавсан -_____________________________________________________________
____________________________________________________________________
____________________________________________________________________
Капрон і найлон -_____________________________________________________
____________________________________________________________________
____________________________________________________________________
Основою рослинних волокон є :_________________________________________ Хімічні волокна виробляють із :_________________________________________
Застосування:________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 49
Біологічно активні речовини
Біологічно активні речовини -__________________________________________
____________________________________________________________________
____________________________________________________________________
До найважливіших речовин цього типу відносять:__________________________
____________________________________________________________________
Вітаміни -___________________________________________________________
____________________________________________________________________
____________________________________________________________________ Вітамін А:___________________________________________________________
Вітамін В1:___________________________________________________________
Вітамін В2:___________________________________________________________
Вітамін В6:___________________________________________________________
Вітамін В12:__________________________________________________________
Вітамін С:___________________________________________________________
Водорозчинні вітаміни -_______________________________________________
____________________________________________________________________
Жиророзчинні вітаміни -_______________________________________________
____________________________________________________________________
Добування вітамінів:__________________________________________________
____________________________________________________________________ ____________________________________________________________________
____________________________________________________________________
Використання:________________________________________________________
____________________________________________________________________
____________________________________________________________________ Ферменти -__________________________________________________________
____________________________________________________________________
____________________________________________________________________
Антибіотики - ________________________________________________________
____________________________________________________________________
____________________________________________________________________
Урок 50
Роль органічної хімії
Органічний синтез -___________________________________________________
____________________________________________________________________
____________________________________________________________________
Органічна хімія і переробка сировини:___________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Органічна хімія і енергетична проблема:__________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Органічна хімія і продовольча проблема:_________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Біотехнології:________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
Органічна хімія і здоров'я людини:_______________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
![]()

про публікацію авторської розробки
Додати розробку

-

Хворостяна Вікторія
06.09.2022 в 12:12
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Дробот Олена Геннадіївна
01.02.2021 в 19:46
Дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Повалихина Лариса
10.04.2020 в 16:41
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Іващенко Любов Іванівна
10.04.2020 в 13:30
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 1 відгук