Роль МАНівських досліджень у подоланні екологічної проблеми
Матеріал містить методичні рекомендації щодо написання МАНівських робіт з хімії та приклади таких робіт. Також розкривається роль таких досліджень у подоланні екологічної проблеми.
1
Роль МАНівських досліджень у подоланні екологічної проблеми
ВСТУП
Із погляду історії, чим цивілізованішою стає людина, тим більший вплив на довкілля вона чинила. На жаль, переважно негативний. А що ж природа? Сьогодні ми спостерігаємо, як вона відповідає нам взаємністю. Ми їй хмару чаду в повітря – вона нам парниковий ефект з цунамі та змінами клімату. Ми нітрати та пестициди на поля – вона нам отруйні овочі та фрукти, небезпечну воду. Ми не закручуємо кранів та не вимикаємо світло – вона іще терпить, але повітря згущується… Схоже на родинну суперечку на кухні, однак ставки багато вищі.
Як змінити такий стан речей? Як відвернути безрадісне майбутнє? Чи означає перераховане вище, що заради примирення слід відмовитися від благ цивілізації: повернутися до натурального господарювання, зректися пральних машин і подорожей на сусідні континенти? Але хто з нас погодиться на таке?
Слід пам’ятати, що кожен із нас щодня робить вибір, руйнівний для світу, перейнявши так званий екологічно дружній спосіб життя. Це – намагання людини залагодити суперечку з природою і не повернутися в печеру.
Бурхливий розвиток хімії та хімічних технологій минулого століття призвели до масового виробництва синтетичних органічних речовин. Багато з них використовують у фармакології, косметиці, як харчові добавки і не мають прямого відношення до навколишнього середовища, але мають суттєвий вплив на здоров’я людей, особливо дітей. Більшість проблем зі здоров’ям людей та техногенним навантаженням на навколишнє середовище обумовлено доступом великої кількості небезпечних хімікатів у довкілля.
Метою навчання хімії є формування засобами навчального предмета ключових компетентностей учнів, необхідних для соціалізації, творчої самореалізації особистості, розуміння природничо-наукової картини світу, вироблення екологічного стилю мислення і поведінки та виховання громадянина демократичного суспільства.
При викладанні хімії в сучасній школі необхідно посилити практичну спрямованість змісту хімічної освіти, акцентуючи увагу на вивченні явищ, процесів, об’єктів, речовин, з якими стикаються учні у повсякденному житті, формувати життєву позицію учнів, їх ціннісну орієнтацію засобами хімії, як навчального предмета, шляхом розуміння користі та шкоди продуктів хімічного виробництва, промислових хімічних процесів, доцільності застосування хімічних продуктів, можливості змінити життя на краще завдяки хімічним знанням.
У пошуках нових підходів до оновлення змісту, форм і методів підготовки вчителя хімії відповідно до формування екологічних компетентностей в першу чергу необхідно враховувати сучасні тенденції розвитку хімічної науки. Серед новітніх напрямів хімії, які з’явились як відгук на глобальні екологічні проблеми, особливе місце займає Зелена хімія.
РОЗДІЛ 1
МАНІВСЬКІ ДОСЛІДЖЕННЯ ЯК ДОПОМОГА У ФОРМУВАННІ ЕКОЛОГІЧНОЇ КУЛЬТУРИ УЧНІВ
Зелена хімія почала бурхливо розвиватися з 90-х років минулого століття.
Основний принцип, на якому базується стратегія і тактика цієї галузі хімічної науки, – скорочення масштабів забруднення навколишнього середовища хімічними речовинами шляхом його запобігання. Але, мабуть, найважливіше тактичне завдання Зеленої хімії – використання відновлюваних ресурсів сировини, зокрема біомаси.
Нові схеми хімічних реакцій і процесів, які розробляються в багатьох лабораторіях світу, покликані кардинально скоротити вплив на навколишнє середовище великотоннажних хімічних виробництв. Хімічні ризики, що неминуче виникають при використанні агресивних середовищ, виробничники традиційно намагаються зменшити, обмежуючи контакти працівників із цими речовинами.
У той же час, Зелена хімія передбачає іншу стратегію – вдумливий відбір вихідних матеріалів і схем процесів, який взагалі виключає використання шкідливих речовин. Таким чином, Зелена хімія – це свого роду мистецтво, що дозволяє не просто отримати потрібну речовину, але отримати її таким шляхом, який, в ідеалі, не шкодить навколишньому середовищу на всіх стадіях його отримання.
Ще один шлях, що веде до цілей Зеленої хімії, – широке використання біомаси замість нафти, з якої хімічні підприємства творять зараз все різноманіття речовин – конструкційні матеріали, хімікати, ліки, парфумерію і багато, багато іншого.
Слід роз'яснити підростаючому поколінню, що нинішній стан навколишнього середовища таїть в собі таку ж небезпеку для людства, як і ядерна війна. Різниця лише в одному – екологічні проблеми більш підступні... Небезпечною помилкою є надія на те, що людство зуміє зупинитися в руйнуванні оточуючого нас світу, коли наблизитися в притул до екологічної загибелі. Буде пізно! В цьому вся підступність проблеми.
Школярів необхідно навчити любити природу, охороняти її та примножувати природні багатства. Прищепити бережливе ставлення до природи, навчити розумно використовувати природні багатства – основна задача екологічного виховання школярів.
Пізнання сутності навколишнього середовища виступає інтегруючою ланкою предметів природничого циклу, і важлива роль у екологізації освіти відводиться навчанню хімії.
Учні також повинні долучатися до вирішення завдань, які ставить перед собою Зелена хімія.
Сьогодні, коли відбувається реформа шкільної освіти, перед сучасною школою постала головна задача створення умов для максимального розвитку природних здібностей кожної дитини, виявлення творчо обдарованих дітей та залучення їх до систематичної науково-дослідницької діяльності.
Вивчення хімії взагалі неможливе без експерименту, тому така дослідницька робота стимулює інтерес до вивчення хімії, допомагає доторкнутися до світу, хоч і маленьких, а все-таки відкриттів. Школярам подобаються завдання творчого характеру, які розвивають у них пізнавальний інтерес: складання казок, кросвордів, ігор; виконання творчих робіт; участь у дослідницьких проектах.
Одним із таких прикладів долучення учнів до основ згаданого напрямку хімії є написання МАНівських робіт.
На першому етапі учні знайомляться з актуальними проблемами теорії та практики конкретної науки, з методологією та методами наукових досліджень, широко залучаються до самостійного вивчення наукової і науково-популярної літератури.
Визначення тематики, вибір учнем об’єкта й предмета дослідження містить у собі другий етап – підготовчий.
Бажано, щоб тема наукової роботи була запропонована самим школярем. На цьому етапі роботи школярі вчаться формувати тему, усвідомлювати її роль у цілісному світоглядному аспекті, визначати конкретні завдання дослідження. Адже чітке формулювання теми й завдань – запорука успіху в процесі творчого пошуку. Учень складає орієнтовний план, в який згодом можуть бути внесені певні корективи.
На підготовчому етапі відбувається збір і систематизація наукових даних. Педагог допомагає школяреві у підборі відповідної літератури. Учень вивчає різні джерела інформації, використовує раніше набуті знання. Самостійна робота учня з літературою є одним з найбільш ефективних засобів розвитку потреби в майбутній самоосвіті.
Основна роль дослідницької роботи полягає в розвитку логічного мислення, умінь інтелектуального проникнення в сутність досліджуваного явища, в пробудженні інтересу до науки, в залученні до пошукової роботи. Ця частина діяльності дає можливість реалізувати визначені експериментальні навички, культуру експериментування школяра.
У ході роботи над експериментальною частиною важливо передбачити варіативність способів виконання експерименту. Учневі необхідно так продумати хід її виконання, щоб мінімізувати витрати сил і часу на одержання максимальної інформації для обробки і осмислення.
Науково-практичні роботи учнів, що набирають необхідну кількість балів під час рецензування, допускаються до усного захисту. Контрольна робота, що супроводжує захист наукової праці, складається із завдань різних рівнів, що не виходить за межі шкільної програми. Оскільки контрольна робота є обов’язковим компонентом для захисту наукової роботи, я готую учнів до виконання цієї роботи
Захист роботи відбувається на науково-практичній конференції під час роботи секцій у присутності учнів і предметного журі. Під час захисту учень називає тему, мету дослідження, план роботи й коротко передає зміст роботи. Особливу увагу слід звернути на практичну частину роботи. Наприкінці виступу учень формулює висновки.
Учитель у ході всіх етапів підготовки виступає не стільки як наставник і керівник, скільки як радник, тим самим створюючи атмосферу співробітництва. Лише за таких умов відбувається звільнення творчих сил дитини, спонукання й підтримка в ній духу пошуку, дослідження, творчості, успіху. А це, напевно, найголовніше, тому що успіх породжує бажання вдосконалюватися.
Мала академія наук України є творчим об’єднанням молоді, що забезпечує її інтелектуальний і духовний розвиток, підготовку до активної діяльності в галузі науки та сприяє самовизначенню в майбутній професії.
Я зі своїм учнем, Морозом Миколою, 3 роки працював над проблемами екологічного характеру. Велику допомогу у вирішенні цього питання нам надавали на кафедрі хімії Національного педагогічного університету імені М.П.Дра-гоманова, зокрема кандидат хімічних наук, доцент та завідувач кафедри хімії Толмачова Валентина Сергіївна та доцент кафедри хімії Ковтун Олена Миколаївна, під керівництвом якої проходила наша робота.
Зараз хочеться навести декілька витягів із наших досліджень.
1.1. Хітин і хітозан – біополімери майбутнього
Наше перше дослідження стосувалося хітину і його тема звучала: “Хітин і хітозан – біополімери майбутнього”.
Виробництво гранул хітозану – це новий напрям у застосуванні полімеру. Гранули на його основі можуть застосовуватись при очищенні води та виконувати роль сорбентів. Гранульована форма полімеру має переваги над порошкоподібною завдяки більшій насипній вазі, а також тому, що гранули можуть бути отримані із заданим вузьким розподілом частинок за розміром, а при достатньо високій дисперсності – зі значно більшою питомою поверхнею, що позитивно позначається на сорбційній здатності хітозану.
Метою роботи було дослідження історії відкриття, будови, властивостей та методів виділення біополімерів хітину та хітозану та їх добування.
Об’єктом дослідження були природні полісахариди хітин і хітозан.
Предметом роботи – дослідження властивостей і методів виділення хітину та хітозану з підмору бджіл.
Завдання дослідження: проаналізувати літературні джерела про будову, властивості та методи виділення хітину та хітозану; експериментально перевірити та удосконалити відому методику виділення хітину та хітозану з підмору бджіл.
Новизна роботи полягає в удосконаленні методики виділення хітину та хітозану з підмору бджіл.
Практичне значення дослідження визначається можливістю впровадження результатів дослідження у виробництво.
Методи дослідження. У роботі використані такі теоретичні методи дослідження: аналіз та узагальнення відповідної літератури і результатів діяльності щодо вивчення даної проблеми; хімічні методи виділення органічних речовин із природної сировини.
Виділення хітину з підмору бджіл. 21,5 г підмору бджіл злегка подрібнили, перенесли в апарат Сокслета для екстракції. Екстрагування проводили петролейним ефіром з температурою кипіння 60-85![]() протягом 10 годин. Після завершення екстракції підмор підсушили на повітрі та знову екстрагували в апараті Сокслета протягом 10 годин 50% водно-спиртовим розчином. Після завершення екстракції підмор сушили на повітрі. Висушений продукт обробили 200 мл 10% розчину натрій гідроксиду протягом 2 годин при температурі 80-90
протягом 10 годин. Після завершення екстракції підмор підсушили на повітрі та знову екстрагували в апараті Сокслета протягом 10 годин 50% водно-спиртовим розчином. Після завершення екстракції підмор сушили на повітрі. Висушений продукт обробили 200 мл 10% розчину натрій гідроксиду протягом 2 годин при температурі 80-90![]() . Під час гідролізу зникали видимі сегменти тіла бджоли. Утворені пластівці хітино-меланінового комплексу темного кольору фільтрували і промивали великою кількістю води до нейтрального середовища промивних вод. Темно-коричневу масу висушували за температури 55
. Під час гідролізу зникали видимі сегменти тіла бджоли. Утворені пластівці хітино-меланінового комплексу темного кольору фільтрували і промивали великою кількістю води до нейтрального середовища промивних вод. Темно-коричневу масу висушували за температури 55![]() . Потім продукт обробили 30% розчином гідроген пероксиду і залишили на 12 годин до повного знебарвлення пластівців. Отриманий хітин промили водою і висушили. В результаті його маса становила 2,5 г, що відповідає 11,63%.
. Потім продукт обробили 30% розчином гідроген пероксиду і залишили на 12 годин до повного знебарвлення пластівців. Отриманий хітин промили водою і висушили. В результаті його маса становила 2,5 г, що відповідає 11,63%.
Добування хітозану. Невелику частину отриманого хітину помістили у пробірку і долили 50% розчин натрій гідроксиду з додаванням кальцинованої соди. Суміш кип’ятили протягом 15 хвилин. Продукт реакції – хітозан – відфільтрували і промили великою кількістю води та висушили.
Щоб переконатися, що було добуто дійсно хітозан, його невелику частину розчинили в розбавленій хлоридній кислоті.
Результати дослідження. Нами було одержано хітин та хітозан із підмору бджіл (Додаток А) та удосконалено методику їх добування.
1.2. Хімія минулого та майбутнього: молочна кислота та полілактиди
Тема нашого другого дослідження звучала: “Хімія минулого та майбутнього: молочна кислота та полілактиди”.
Саме на основі молочної кислоти проводяться дослідження по розробці умов олігомеризації молочної кислоти, отримання циклічного лактида і перетворення його в полімолочну кислоту.
При розробці процесу олігомеризації 85% водної молочної кислоти на першій стадії відпрацьовувався спосіб відгонки води при нагріванні суміші до температури 125ºС при нормальному тиску. При цьому вода легко відганялася до отримання 90 – 95% розчину молочної кислоти. Подальша відгонка води була ускладнена, тому для її видалення застосовували вакуум із барботуванням сухого азоту через розчин молочної кислоти.
Процес видалення води в лабораторних умовах у вакуумі відбувався 3 – 5 год. При цьому в реакторі залишалась безводна молочна кислота. Це вказує на те, що при відгонці води в запропонованому режимі починався процес олігомеризації із утворенням незначної кількості димерних і тримерних продуктів конденсації молочної кислоти. Теоретичне значення кислотного числа мономерної молочної кислоти дорівнює 623 мг КОН/г продукту.
Було відмічено, що при відгонці води спостерігався помітний виніс молочної кислоти, особливо на заключній стадії, коли процес проводився у вакуумі. Кислотність водного погону протягом відгонки коливалась від 5 до 20 мг КОН/г. У відігнаній воді містилася молочна кислота в кількості до 3% по масі загального завантаження. У промислових умовах цю кислоту необхідно регенерувати і повертати в технологічний процес.
Проведення чисто термічної поліконденсації молочної кислоти при атмосферному тиску і температурі 100 – 110 С забезпечує одержання низькомолекулярного олігомера із середнім ступенем полімеризації. У зв’язку із цим проводилися ряд досліджень по використанню різноманітних каталітичних систем поліконденсації молочної кислоти із метою отримання олігомерів із заданою молекулярною масою 800 – 1200.
У якості каталізаторів вивчалися різноманітні за природою системи: оксид цинку і пара-толуенсульфокислота.
Отримання полілактиду за участю цинк оксиду. При дослідженні цинк оксиду в якості каталітичної системи олігомеризації процес проводився при поетапному підвищенні температури.
До зневодненої молочної кислоти помістили 1,5% цинк оксиду, набирався вакуум і система нагрівалася до 115 – 120ºС із постійним барботуванням сухого азоту. Після двогодинного нагрівання реакційної маси її кислотне число дорівнювало 150 мг КОН/г продукту.
З метою підвищення ступеня поліконденсації молочної кислоти температуру реакційної маси підвищували до 150 – 170°С і продовжували нагрівання ще 2,5 год. За час реакції олігомеризації у присутності ZnO в приймачі із водою збиралося 20% за масою загального завантаження молочної кислоти із кислотністю 260 мг КОН/г продукту. Це свідчить про те, що, окрім реакційної води, відбувався виніс молочної кислоти та її низькомолекулярних олігомерів.
Незважаючи на досить жорсткі умови олігомеризації у присутності каталізатора ZnO, все-таки не змогли отримати олігомер молочної кислоти із молекулярною масою, оптимальною для одержання лактида.
Отримання полілактиду за участю пара-толуенсульфокислоти. Для досягнення необхідного ступеня поліконденсації молочної кислоти в якості каталізатора олігомеризації дослідили пара-толуенсульфокислоту, яка широко застосовується для одержання складних ефірів на основі карбонових кислот і спиртів. Реакція олігомеризації молочної кислоти у присутності 0,5 – 2% пара-толуенсульфокислоти проводилася в середовищі азеотропуючих розчинників.
Досліди із використанням у якості розчинника циклогексану і 0,5% каталізатора проводилися при 80 – 85ºС, однак виділення води при цьому не спостерігалось. Із цієї причини циклогексан був замінений на більш висококиплячий розчинник – толуен і кількість каталізатора збільшили до 1 – 2%. За цих умов одержали олігомер із середнім ступенем поліконденсації 10 – 15, що відповідало молекулярній масі 720 – 1100.
Отримання лактида та полілактиду. Процес лактидизації одержаних олігомерів проводять в присутності свіжо-виготовленого цинкового пилу в реакторі, обладнаному термометром, насадкою Вюрца, з’єднаною із низхідним холодильником та із приймачем. Після завантаження олігомера, що містить 2% каталізатора лактидизації, в системі набирали вакуум і повільно підвищували температуру реакційної маси до 170 – 190ºС. При цьому в приймачі, охолодженому льодом, конденсувався світло-жовтий продукт.
Із метою очистки одержаного лактиду-сирцю його перекристалізували із етилацетату і одержали білі кристалики із температурою плавлення 94,8ºС.
Отримане значення температури плавлення близьке до літературних даних для лактида, що вказує на відсутність процесу рацемізації вихідної молочної кислоти. Збереження оптичної чистоти лактида є важливим показником, так як біодеградуючі полімери, отримані на основі молочної кислоти, мають більш кращі фізико-механічні властивості у порівнянні із оптично неактивними аналогами.
Перекристалізований і висушений оптично активний лактид у подальшому було використано як вихідний продукт під час одержання полімолочної кислоти за присутності станум диоктаноату як каталізатора полімеризації (Додаток Б).
Метою роботи було дослідження історії відкриття, будови, властивостей та методів виділення молочної кислоти та біополімеру полілактиду та їх добування.
Об’єктом дослідження було природні молочна кислота та полілактид.
Предметом роботи – дослідження властивостей і методів виділення молочної кислоти та полілактиду.
Завдання дослідження: проаналізувати літературні джерела про будову, властивості молочної кислоти та полілактиду, створити методику виділення 2-гідроксипропіонової кислоти із молочної сироватки та синтезувати полілактид.
Новизна роботи полягає в створенні методики виділення 2-гідроксипро-піонової кислоти із молочної сироватки.
Методи дослідження. У роботі використані такі теоретичні методи дослідження: аналіз та узагальнення відповідної літератури і результатів діяльності щодо вивчення даної проблеми; хімічні методи виділення органічних речовин із природної сировини.
Результати дослідження. Нами було одержано молочну кислоту і полілактид та удосконалено методику їх добування (Додаток В).
Практичне значення дослідження визначається можливістю впровадження результатів дослідження у виробництво.
1.3. Хітин, полілактати та дигідрокверцетин як сучасні, перспективні та актуальні об’єкти дослідження Зеленої хімії
Третя тема, яка була підсумком нашої трирічної співпраці і, разом з тим, об’єднувала дві попередні роботи звучала так: “Хітин, полілактати та дигідрокверцетин як сучасні, перспективні та актуальні об’єкти дослідження Зеленої хімії”.
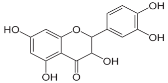
Методика виділення дигідрокверцетину із деревини модрини сибірської (сосни). До подрібненої деревини та кори модрини сибірської (сосни) додають етанол і екстрагують кип’ятінням протягом 2 годин. Після відгонки спирту екстракт обробляють петролейним ефіром для видалення із нього сторонніх домішок та отримання основної кількості дигідрокверцетину.
Одержання дигідрокверцетину із деревини модрини сибірської (сосни). 20 г деревини та кори модрини сибірської (сосни) подрібнили і помістили у колбу. В колбу налили 200 мл 75% розчину етанолу. Суміш про екстрагували протягом 2 годин. Потім відфільтрували і відігнали спирт. Екстракт обробили петролейним ефіром та отримали дигідрокверцетин.
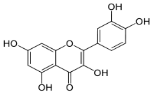
Методика одержання кверцетину з дигідрокверцетину. До дигідрокверцетину додають сухий натрій сульфіт. Доливають спирту до мітки 100мл. Отриманий розчин кип’ятять протягом 2 годин. Розчин охолоджують, відфільтровують і висушують. В результаті отримують кверцетин.
Одержання кверцетину з дигідрокверцетину. До 15г дигідрокверцетину додали 15г сухого натрій сульфіту. Долили спирт до мітки 100 мл. Отриманий розчин кип’ятили протягом 2 годин. Розчин охолодили, відфільтрували та висушили. Отримали кверцетин (Додаток Г).
Na2SO3
Метою роботи було дослідження історії відкриття, будови, властивостей і методів виділення біополімерів хітину та хітозану, молочної кислоти, біополімеру полілактиду, кверцетину та дигідрокверцетину та їх добування.
Об’єктом дослідження – природні полісахариди хітин і хітозан, молочна кислота та полілактид, кверцетин та дигідрокверцетин.
Предмет роботи – дослідження властивостей і методів виділення хітину та хітозану з підмору бджіл, молочної кислоти та полілактиду, кверцетину та дигідрокверцетину із деревини модрини сибірської та сосни звичайної.
Завдання дослідження: проаналізувати літературні джерела про будову, властивості та методи виділення хітину та хітозану, молочної кислоти і полілактиду, кверцетину та дигідрокверцетину, експериментально перевірити та удосконалити відому методику виділення хітину та хітозану з підмору бджіл, створити методику виділення 2-гідроксипропіонової кислоти із молочної сироватки, синтезувати полілактид, добути кверцетин та дигідрокверцетин із деревини модрини сибірської та сосни звичайної.
Новизна роботи полягає в удосконаленні методики виділення хітину та хітозану з підмору бджіл, у створенні методики виділення 2-гідроксипропіоно-вої кислоти із молочної сироватки та у виділенні кверцетину та дигідрокверцетину з кори та деревини модрини сибірської.
Методи дослідження. У роботі використані такі теоретичні методи дослідження: аналіз та узагальнення відповідної літератури і результатів діяльності щодо вивчення даної проблеми; хімічні методи виділення органічних речовин із природної сировини.
Результати дослідження. Нами було одержано хітин та хітозан із підмору бджіл, молочну кислоту і полілактид, кверцетин та дигідрокверцетин та удосконалено методику їх добування.
Практичне значення дослідження визначається можливістю впровадження результатів дослідження у виробництво.
Тож мій досвід показує, що виконання наукових робіт учнями в галузі Зеленої хімії сприяє формуванню нового екологічного мислення, нового бачення процесів, що відбуваються на Землі. Тому пробуйте та дерзайте! Творчих успіхів вам і нових відкриттів!
ВИСНОВКИ
Згідно з метою роботи можна зробити наступні висновки:
1) нами було одержано: хітин та хітозан із підмору бджіл та удосконалено методику їх добування; 2-гідроксипропіонову кислоту із молочної сироватки та полілактид, а також створено методику виділення цієї кислоти із молочної сироватки; кверцетин та дигідрокверцетин з кори модрини сибірської та сосни;
2) у разі проникнення в людський організм хітин постійно активізує перистальтику кишечника, сприяючи безпечному схудненню; хітин і його похідні – чудовий матеріал для виготовлення штучної шкіри, плівок і мембран, а також ефективний біологічний фільтр, що забезпечує зв’язування і виведення з організму шкідливих продуктів життєдіяльності;
4) здатність хітозану утворювати плівки для збереження вологості, зменшення числа бактерій, продовження життя шкірки у продуктів, що швидко псуються, покладено в основу препаратів, які підвищують термін зберігання плодоовочевої продукції;
5) ПЛ відповідає усім технічним вимогам, що стосуються пакувальних матеріалів. Тому полілактати є кращою альтернативою традиційним пластикам із точки зору необхідності різкого скорочення кількості пластикового сміття, що завозиться на муніципальні звалища;
6) волокна, отримані із PLA, не поступаються по міцності волокнам, одержаним із інших поліефірів, і є стійкими до гідролізу навіть у киплячій воді та добувається із природної сировини – зерна або цукру. Продукти біодеструкції волокон із PLA не шкідливі для організму та навколишнього середовища. Використання PLA у медицині обмежено виготовленням кісткових протезів, кісткових гвинтів та імплантатів для кісткових тканин;
7) біофлавоноїди, зокрема кверцетин та дигідрокверцетин, – група біологічно активних речовин, які підтримують еластичність капілярів, зміцнюють їх стінки та зменшують проникність. Вони не синтезуються ні в тканинах тварин, ні кишковою мікрофлорою, вони синтезуються виключно в клітинах рослин;
8) основним джерелом дигідрокверцетину є деревина модрини сибірської. Вона містить до 2,5% флавоноїдів, при цьому вміст дигідрокверцетину сягає 90%;
9) кверцетин є сильним антиоксидантом, проявляє антиалергічну та імуностимулюючу дію, блокує дію деяких ферментів, має протинабрякову, спазмолітичну, антигістамінну, протизапальну дію;
10) дигідрокверцетин має потужну антиоксидантну дію, перешкоджає шкідливій дії вільних радикалів, гальмує процеси пероксидного окиснення ліпідів клітинних мембран і ліпопротеїдів сироватки крові, покращує внутрішньотканинне дихання, зменшує проникність і ламкість капілярів, покращує мікроциркуляцію й коронарний відтік, сприяє нормалізації збудливості й провідності серцевого м’яза, гальмує передчасне старіння клітин і розвиток різних захворювань;
11) хітин, хітозан, полілактид та полілактати, кверцетин та дигідрокверцетин є сучасними, перспективними та актуальними об’єктами дослідження зеленої хімії;
12) результати нашого дослідження можна впроваджувати у виробництво;
13) отже, саме МАНівські дослідження із хімії допоможуть зрозуміти і подолати всі ті екологічні негаразди, які людство відчуває на собі ось вже впродовж кількох десятиліть. Звичайно, до цього потрібно підійти цілком виважено. Школярів необхідно навчити любити природу, охороняти її та примножувати природні багатства. Пізнання сутності навколишнього середовища виступає інтегруючою ланкою предметів природничого циклу, і важлива роль у екологізації освіти відводиться навчанню хімії.
Прищепити бережливе ставлення до природи, навчити розумно використовувати природні багатства – основна задача екологічного виховання школярів. Виконання наукових робіт учнями в галузі Зеленої хімії сприяє формуванню нового екологічного мислення, нового бачення процесів, що відбуваються на Землі.
Мала академія наук України є творчим об’єднанням молоді, що забезпечує її інтелектуальний і духовний розвиток, підготовку до активної діяльності в галузі науки та сприяє самовизначенню в майбутній професії.
СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ
1. Л.А. Алешина, С.В. Глазков, Л.А. Луговская, М.В. Подойникова, А.Д. Фосфанов, Е.В. Силина. Современные представления о строении целлюлоз (обзор) // Химия растительного сырья. 2001. №1. С.5-36.
2. Бабкін В.А., Остроумова Л.А., Дьячкова С.Г., Святкін Ю.К, Бабкін Д.В., Онучіна Н.А. Безвідходна комплексна переробка біомаси модрини сибірської і даурської // Хімія в інтересах сталого розвитку. 1997. №5. С.105-115.
3. Быкова В.М., Немцев С.В. Сырьевые источники и способы получения хитина и хитозана // Хитин и хитозан: Получение, свойства и применение. – М.: Наука. – 2002. – С.7-22.
4. Горовой Л.Ф. Косяков В.Н. Сорбционные свойства хитина и его производных // Хитин и хитозан: Получение, свойства и применение. – М.: Наука. – 2002. – С.217-240.
5. Куприна Е.Э. Водолажская С.В. Способы получения и активации хитина и хитозана // Хитин и хитозан: Получение, свойства и применение. – М.: Наука. – 2002. – С.44-61.
6. Ластухін Ю.О. Хімія природних сполук: Навчальний посібник. – Львів: Національний університет «Львівська політехніка» (інформаційно-видавничий центр «ІНТЕЛЕКТ+» Інституту післядипломної освіти) «Інтелект-Захід». – 2005. – 560с.\
7. Левданський В.А., Полежаєва Н.І., Кузнєцов Б.Н. Спосіб отримання кверцетину // Патент РФ 2182906.2002.
8. Максютина Н.П. Рослинний антиоксидант кверцетин та перспективи його використання в медицині // Фармацевтичний журнал. 1993. №4. С.80-83.
9. Максютина Н.П., Комиссаренко Н.Ф., Прокопенко А.П. и др. / Под ред. Н.П. Максютиной. Растительные лекарственные средства // К.: Здоровье. 1985. 280с.
10. Немцов С.В., Зуева О.Ю., Хисматуллин Р.Г. и др. // Пчеловодство. – 2001. − №5.
11. Нудьга Л.А. Производные хитина и хитозана и их свойства // Хитин и хитозан: Получение, свойства и применение. – М.: Наука. – 2002. – С.141-177.
12. Перепелкин К.Е. // Химия и химическая технология волокон. 2002. №.2.
13. Попов А.В. // Тара и упаковка. 2007. №3.
14. Робота з обдарованими учнями. Хімічна секція МАН / Упоряд. К.М.Задорожний – Х.: Вид. група “Основа”, 2005. – 96с. – (Б-ка журн. “Хімія”; Вип. 12 (36)).
15. Сирів В.Ф., Хушбакатова З.А., Гукасов В.М. та ін. Антиоксидантна активність деяких рослинних фенольних сполук // Хіміко-фармацевтичний журнал. 1987. Т.21. №1. С.59-61.
16. Солодовнік Т.В., Куриленко Ю.М., Омельчук С.В. Одержання та фотометричне дослідження хітозану з ракоподібної сировини // Вісник ЧДТУ. – 2009. − №4. – С.100-103.
17. Фомин В.А., Гузеев В.В. // Пластические массы. 2001. № 2.
18. Хитин и хитозан: Получение, свойства и применение / Под ред. К.Г Скрябина, Г.А. Вихоревой, В.П. Варламова. – М.: Наука. – 2002. – 368с.: ил.
19. Чирков С.Н. Противовирусные свойства хитозана // Хитин и хитозан: Получение, свойства и применение. – М.: Наука. – 2002. – С.327-336.
ІНТЕРНЕТ-РЕСУРСИ
http: // www.chitin.ru / history.htm
http://b2blogger.com/articles/review/202.html
http://go.mail.ru/search_images?q=молочная+кислота&rch
http:newchemistry.ru/letter.php?nid=8221
http:uk.wikipedia.org/wiki/Молочна кислота
http:upakovano.ru/articles/2723упаковка
http:ru.wikipedia.org/wiki/Полилактид
Додаток А

Додаток Б
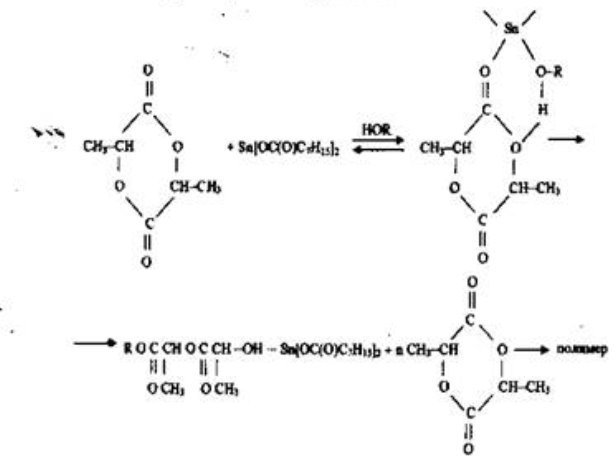
Полімеризація в полімолочну кислоту в присутності станум диоктаноату
Додаток В

Додаток Г




про публікацію авторської розробки
Додати розробку