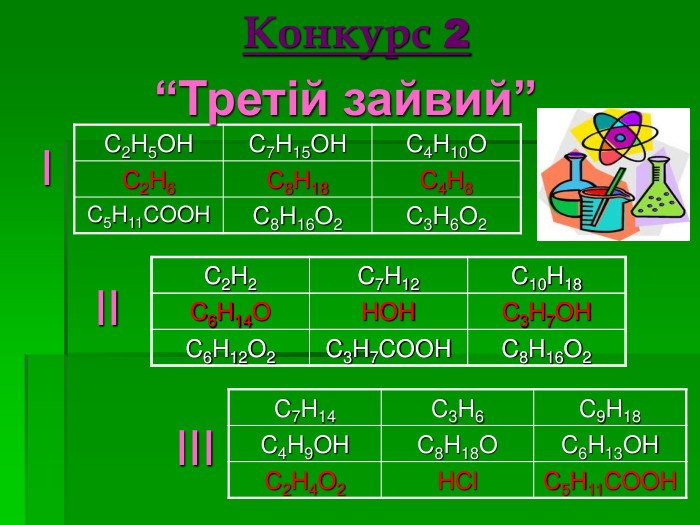
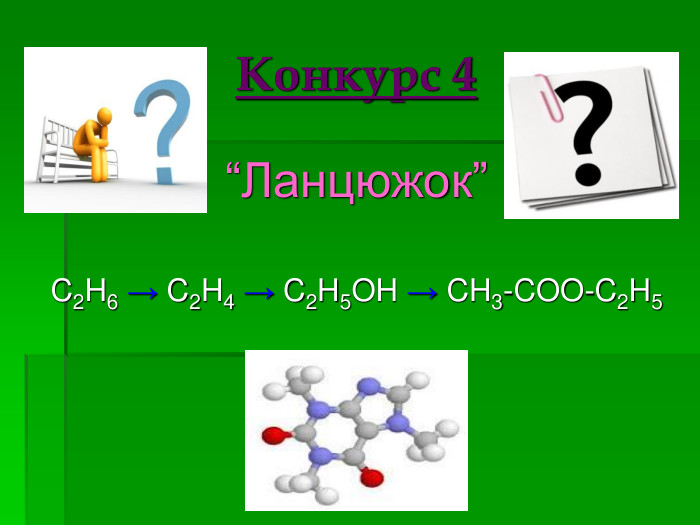
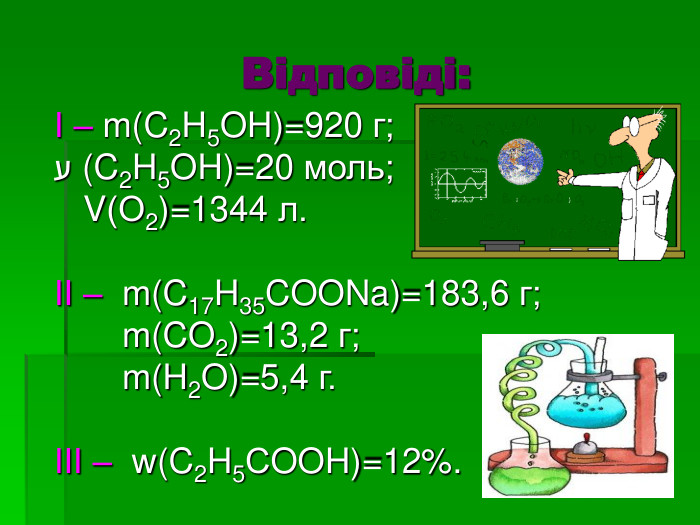
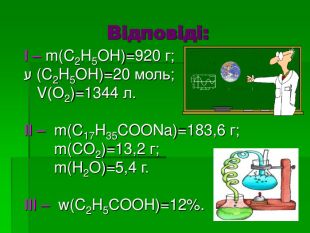
Спирти. Карбонові кислоти. Жири
Про матеріал
Повторити та узагальнити основні поняття спиртів, карбонових кислот, жирів; розширити уявлення працювати в групі. Формувати вміння аналізувати та робити висновки із життя. Закріпити навички розв'язувати задачі та вправи різних типів Перегляд файлу
Зміст слайдів
ppt
До підручника
Хімія 9 клас (Савчин М.М.)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку