.Урок "Хімія та математика навколо нас"
- Урок.docx docx
- Хімія і матем.ppt ppt
Хімія та математика навколо нас
Усі науки так пов’язані між собою,
що легше їх вивчати всі разом,
аніж кожну окремо.
Рене Декарт
Формування ключових компетентностей:
- комунікативної: працюючи в групі, уміти швидко і якісно орієнтуватися в запропонованих завданнях;
- спілкуватися державною мовою;
- уміння вчитися впродовж життя;
- соціально-трудової — уміння оперувати знаннями, розвивати гнучкість отриманих знань, робити висновки й узагальнення.
Формування предметних компетентностей:
- математичні: узагальнити й систематизувати знання учнів із теми «Відношення і пропорції. Відсоткове відношення двох чисел», удосконалити вміння розв'язувати задачі;
- хімічні: познайомити учнів із хімічними речовинами, дослідами, хімічною реакцією, правилами розв'язання розрахункових задач із хімії.
Наскрізні лінії: екологічна безпека і сталий розвиток.
Мета інтеграції: показати учням цілісність навколишнього середовища, тематичну залежність предметів, єдність математики з іншими природничими дисциплінами; підготувати учнів до сприйняття інших навчальних предметів у наступних класах.
Тип уроку: застосування знань.
Обладнання: підручник, мультимедійний проектор, презентація, роздавальний матеріал — картки дослідника, лоток із хімічними речовинами: солі (кухонна сіль, мідний купорос, сода харчова), вода; посуд: хімічна склянка, скляна паличка, ложечки (різні за розміром)
Форми роботи: робота в гетерогенних групах, прийоми «Мозкова атака», «Склади слово», «Математичний крос», «Дослідницька лабораторія», робота в групах, бесіда, демонстрація.
ХІД УРОКУ
- ОРГАНІЗАЦІЯ КЛАСУ
- ОГОЛОШЕННЯ ТЕМИ Й МЕТИ УРОКУ
ІІІ. АКТУАЛІЗАЦІЯ ОПОРНИХ ЗНАНЬ (МАТЕМАТИЧНИХ)
Прийом «Мозкова атака»
- Що називається відношенням двох чисел?
- Що таке пропорція?
- Як знайти невідомий крайній член пропорції?
- Сформулюйте основну властивість пропорції.
ПРОПОРЦІЯ ПРИЗНАЧИТЬ ВАМ ПОБАЧЕННЯ НА УРОКАХ: алгебри, геометрії, фізики, біології, географії, креслення та музики
Прийом «Склади слово»
Усний рахунок: знайти невідомий член пропорції.
|
50 |
16 |
10 |
16 |
8 |
|
X |
І |
М |
І |
Я |
х: 16 = 2:4; 2 : 5 = 4 : х; 8 : х = 1: 2; 5 : 9 = х : 90
ІV. МОТИВАЦІЯ НАВЧАЛЬНОЇ ДІЯЛЬНОСТІ
Демонстрація презентації: «Хімія навколо
нас», бесіда за презентацією
Хімія — захоплива наука. Вивчати її необхідно для того, щоб розуміти, як побудований навколишній світ і за якими законами він розвивається, щоб використовувати різні речовини, не завдаючи шкоди собі, не руйнуючи природу, а оберігаючи й примножуючи її багатства.
Хімія — наука про речовини, їх властивості та перетворення. Головним об’єктом вивчення є речовини, що вступають у різні перетворення. Такі перетворення називаються хімічними реакціями.
Для проведення реакції потрібно знати, яку масу речовини взяти, щоб отримати потрібну концентрацію. Поняття «пропорція» дуже активно використовується в хімічній науці для ведення розрахунків, а також для виявлення концентрації розчинів.
Запитання: що таке розчин? (суміш, що складається з речовини й розчинника — води).
- А як можна виразити кількісний склад
розчину?
Щоб дізнатися про кількісний склад розчину, вдамося до математичних обчислень, зокрема до обчислення масової частки речовини (концентрації) в розчині.
Концентрація — величина, що характеризує кількісний склад розчину.
Масова частка розчиненої речовини в розчині (W%) — це відношення маси розчиненої речовини (т 1) до маси розчину (т2).
Матеріал уроку ви будете використовувати при розв’язанні розрахункових задач на уроках хімії. Сьогодні ж ми будемо перетворювати одні речовини на інші.
Задача
Взаємоперетворення кристалогідрату мідного купоросу
При нагріванні кристалогідрати розкладаються з виділенням води, вони перетворюються на безводну речовину. Запишемо рівняння реакції:
СuSО4 • 5Н2O →СuSО4 + 5Н2O та складемо співвідношення однотипних величин:
90 г СuSО4 • 5Н2O — 60 г СuSО4
120 г СuSО4 • 5Н20 — ? СuSО4
пропорція:
90 г — 60 г
120 г — х г
Яку залежність між масою речовини, що вступила в реакцію, та масою утвореного продукту реакції ви з’ясуєте за даними досліду?
Яку пропорцію ви складете?
Яку властивість ви використали?
![]() =
= ![]()
х = ![]()
х = 80
V. ЗАКРІПЛЕННЯ Й ОСМИСЛЕННЯ ЗНАНЬ І НАВИЧОК
1. Дослідницька лабораторія
Ми пропонуємо вам на деякий час стати співробітниками наукової лабораторії. Кожна лабораторія отримує своє завдання для експерименту і проводить його в групі, дотримуючись правил безпеки.
Робота в групах
Виберіть керівника лабораторії, лаборанта.
Карта дослідника № 1
Мідний купорос (СuSO4) — кристалічна речовина блакитного кольору. Застосування:
- у садівництві для знищення паразитів на рослинах;
- для боротьби з пліснявою;
- у будівництві;
- у лікувальній сфері.
Задача
Виготовлення розчину мідного купоросу з певною масовою часткою розчиненої речовини
- У склянку з водою масою 200 г насипаємо 8 г мідного купоросу, перемішуємо (скляною паличкою) до повного розчинення.
- Знаходимо загальну масу води та мідного купоросу в розчині (г).
- Запишемо відношення маси мідного купоросу до маси розчину. (Відношення маси мідного купоросу до маси розчину називається масовою часткою розчиненої речовини).
- Обчислюємо масову частку розчиненої речовини в розчині (відповідь округлюємо до сотих).
- Відповідь округлюємо до сотих і виражаємо у відсотках.
- А якщо у склянку з водою масою 200 г додамо 4 г мідного купоросу, якою буде концентрація розчину?
- Можна зробити такий висновок: якщо зменшується кількість речовини, то зменшується концентрація розчину. Отже, це пряма пропорційна залежність.
Карта дослідника № 2
Сода харчова (NaHCO3) – речовина білого кольору, розчинна у воді.
Застосування:
- приготування їжі(тісто);
- видалення бруду;
- косметологія;
- медицина (розчин для полоскання горла, носа, інгаляції).
Задача
- У склянку з водою масою 250 г насипаємо 1 чайну ложку соди (це 5 г), перемішуємо (скляною паличкою) до повного розчинення.
- Знаходимо загальну масу води та соди в розчині (г).
- Запишемо відношення маси соди до маси розчину. (Відношення маси соди до маси розчину називається масовою часткою розчиненої речовини).
- Обчислюємо масову частку розчиненої речовини в розчині
- Відповідь округлюємо до сотих і виражаємо у відсотках.
Карта дослідника № 3
Цукор (С12Н22О11) — кристалічна речовина білого кольору.
Застосування:
- в харчовій промисловості (в кондитерських виробах, компотах, вареннях, консервації,..);
- у фармакології (при виготовленні пігулок та сиропів).
Задача
Приготування ранкового чаю з цукром.
- У склянку з водою масою 250 г насипаємо дві ложки цукру, перемішуємо (ложкою) до повного розчинення. Маса однієї ложки цукру дорівнює 10 г.
- Знаходимо загальну масу води та цукру в розчині (г).
- Запишемо відношення маси цукру до маси розчину. (Відношення маси цукру до маси розчину називається масовою часткою розчиненої речовини).
- Обчислюємо масову частку розчиненої речовини в розчині .
- Відповідь округлюємо до сотих і виражаємо у відсотках.
- Який інший спосіб обчислення концентрації речовини у розчині ви знаєте?
Дослідницька лабораторія продовжує працювати
Кухонна сіль (N801) — кристалічна речовина білого кольору.
Застосування:
- приправа в харчовій промисловості;
- антисептик (убиває мікроби);
- при виробництві мила;
- у медицині (0,9 % розчин) — фізіологічний розчин.
2. Робота в групах
Задача 1
До 400 г 14% розчину солі додали 30 г солі.
Знайдіть відсотковий вміст солі в новому розчині.
|
|
% |
Маса розчину |
Маса речовини
|
|
І розчин |
|
|
|
|
ІІ розчин |
|
|
|
Задача 2
До 400 г 14% розчину солі додали 300 г води.
Знайдіть відсотковий вміст солі в новому розчині.
|
|
% |
Маса розчину |
Маса речовини
|
|
І розчин |
|
|
|
|
ІІ розчин |
|
|
|
Задача 3
Із 600 г 8% розчину солі випарували 200 г води.
Знайдіть відсотковий вміст солі в новому розчині.
|
|
% |
Маса розчину |
Маса речовини
|
|
І розчин |
|
|
|
|
ІІ розчин |
|
|
|
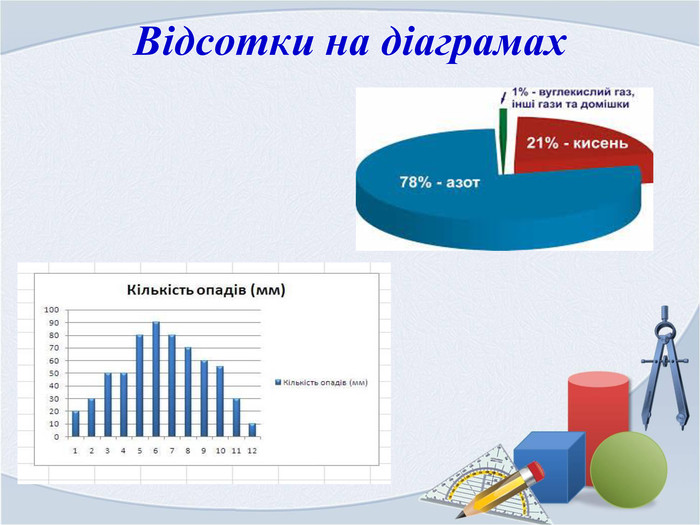
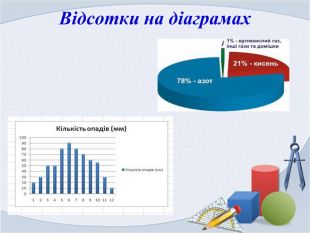
3. Відсотки на діаграмах. Побудова кругової діаграми.
На кругових діаграмах зручно подавати дані у відсотках.
Робота в групах
Задача 1. Повітря складається з кисню – 20,94%, азоту – 79,03% і вуглекислого газу - 0,03%. Побудувати кругову діаграму.
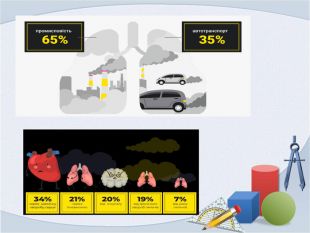
Задача 2. Основні чинники забруднення повітря: промислові підприємства – 60%, автотранспорт – 30% , інше(пожежі, спалювання листя) – 10%. Побудувати кругову діаграму.
Задача 3. Вплив забрудненого повітря на здоров’я людини: серцево-судинні захворювання - 45%, захворювання дихальної системи - 40 %, інші захворювання (шкіри, органів слуху та ін.) - 15%.
VІ. Підсумок уроку
Отже, ви дізналися , що пропорція – це не тільки математична величина.
- З яким предметом ми сьогодні пов’язали математику?
- А де ще можна застосовувати пропорцію?
- Чи зможете ви застосувати отримані знання на практиці?
- Які труднощі виникли у вас при розв’язуванні задач?
Діти, я хочу дізнатися про ваш настрій після уроку. Виходячи з класу, приклейте стікер на той смайлик, який відповідає вашому настрою. Можна написати свої враження або побажання.
VІ. Домашнє завдання
Складіть вдома аналогічну задачу для дослідження із будь-якої галузі чи сфери життя людини.


про публікацію авторської розробки
Додати розробку