ПЛАН-КОНСПЕКТ УРОКУ У 9 КЛАСІ БІОЛОГО-ХІМІЧНОГО ПРОФІЛЮ НА ТЕМУ: «ДОСЛІДЖЕННЯ ХІМІЧНИХ ВЛАСТИВОСТЕЙ ОЦТОВОЇ КИСЛОТИ. ЗАСТОСУВАННЯ ОЦТОВОЇ КИСЛОТИ»
Мета уроку: Ознайомити учнів із хімічними властивостями оцтової кислоти, а саме розглянути електролітичну дисоціацію оцтової кислоти, взаємодію з металами, лугами, солями, спиртами, оксидами. Навчити учнів складати відповідні рівняння реакцій. Вияснити, яким чином можна виявити оцтову кислоту (продемонструвати на досліді), та де її застосовують.
Міністерство освіти і науки України
Рівненський природничо-математичний ліцей «Елітар»
Рівненської міської ради
ПЛАН-КОНСПЕКТ УРОКУ У 9 КЛАСІ
БІОЛОГО-ХІМІЧНОГО ПРОФІЛЮ НА ТЕМУ:
«Дослідження хімічних властивостей оцтової кислоти. Застосування оцтової кислоти»

Розробив: учитель хімії,
ПМЛ «Елітар»
ДАНИЛЮК РОМАН ЕДУАРДОВИЧ
Рівне - 2013
Нестандартний урок у 9 класі біолого-хімічного профілю
Тема уроку: «Дослідження хімічних властивостей оцтової кислоти. Застосування оцтової кислоти».
Мета уроку: Ознайомити учнів із хімічними властивостями оцтової кислоти, а саме розглянути електролітичну дисоціацію оцтової кислоти, взаємодію з металами, лугами, солями, спиртами, оксидами. Навчити учнів складати відповідні рівняння реакцій. Вияснити, яким чином можна виявити оцтову кислоту (продемонструвати на досліді), та де її застосовують.
Тип уроку: Урок-дослідження.
Обладнання: мультимедійний проектор, презентація «Хімічні властивості оцтової кислоти»
План уроку:
І. Організація класу
ІІ. Актуалізація опорних знань.
Пригадайте?
- Що називають функціональною групою? Які функціональні групи ви знаєте?
- Які сполуки називаються карбоновими кислотами? На які типи вони поділяються і за якими ознаками?
- Які представники карбонових кислот вам відомі? Назвіть їх.
ІІІ. Оголошення теми та мети уроку.
ХІМІЧНІ ВЛАСТИВОСТІ ОЦТОВОЇ КИСЛОТИ.
ЗАСТОСУВАННЯ ОЦТОВОЇ КИСЛОТИ
ІV. Мотивація навчальної діяльності
Історія відкриття оцтової кислоти
Знайома людям з давніх часів:
- Оцет виготовлявся людиною ще в давні часи.
- Про практичне його застосування вперше згадується у ІІІ ст. до н. е.
- Грецький вчений Теофраст вперше описав дію оцту на метали.
- Оцет застосовувався для добування свинцевих білил.
Отруйна сапа ?
- В Стародавньому Римі вино тримали у свинцевому посуді. При цьому отримували дуже солодкий напій – сапу.
- Сапа містила велику кількість ацетату плюмбуму — дуже солодкої речовини, яку називають «свинцевим цукром» або «цукром Сатурна». Популярність сапи була причиною хронічного отруєння свинцем серед римської аристократії.
Вклад арабських алхіміків:
- В VIII ст. арабський алхімік Джабир ібн Хайян вперше отримав концентровану оцтову кислоту шляхом перегонки.
- За часів Епохи Відродження льодяну оцтову кислоту добували перегонкою ацетатів деяких металів (наприклад, ацетат купруму (II)).
V. Дослідження оцтової кислоти з елементами реклами.
Лабораторний дослід №13. Дія оцтової кислоти на індикатори
Лабораторний дослід №14. Взаємодія оцтової кислоти з металами, лугами, солями
VI. Застосування Оцтової кислоти:
Вдома учні підготували інформацію про застосування оцтової кислоти у вигляді реклами. На уроці обговорюємо застосування і записуємо основні тези в бланк дослідження.
VII. Домашнє завдання:
1. Опрацювати § 27. (П.П.Попель, Л.С.Крикля, Хімія – 9).
- І група учнів (оцінка 7-9), виконати вправи 239, 240. с. 162.
ІІ група учнів (оцінка 10-11), вправи 241, 245 с.162, 163.
3. Творче завдання: Написати казку “Подорож оцтової кислоти”.
КАРТКА УРОКУ-ДОСЛІДЖЕННЯ
П.І.Б. ______________________ Клас __________ ОЦІНКА _______________________
ТЕМА: Хімічні властивості оцтової кислоти.
Застосування оцтової кислоти.
Пригадайте?
- Функціональна група - __________________________________________________________
_________________________________________________________________________________________________________________________________________________________________________
- Класифікація карбонових кислот - __________________________________________________
_____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
- Окремі представники карбонових кислот - _________________________________________
______________________________________________________________________________________________________________________________________________________________________________
Історія відкриття оцтової кислоти _______________________________________________________
_________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
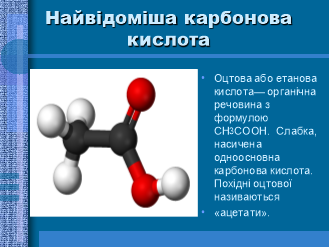
Фізичні властивості оцтової кислоти ____________________________________________________
__________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
ДОСЛІДЖУЄМО ХІМІЧНІ ВЛАСТИВОСТІ ОЦТОВОЇ КИЛОТИ:
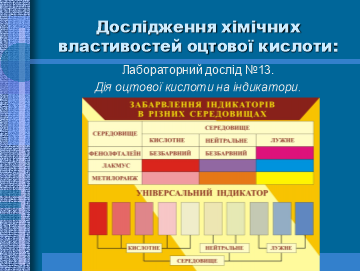
Лабораторний дослід №13. Дія оцтової кислоти на індикатори.
Інструктаж з БЖД.
Реактиви: розчин оцтової кислоти 6%, універсальний індикаторний папір, розчини індикаторів фенолфталеїну, метилоранжу, лакмусу.
Обладнання та хімічний посуд: штатив з пробірками, скляна паличка
Порядок виконання: У 4 пробірки налийте по 1 мл розчину оцтової кислоти, в 1 пробірку долийте розчин фенолфталеїну, в 2 пробірку – метилоранжу, в 3 пробірку розчин – лакмусу а в 4 пробірку – киньте універсальний індикаторний папірець. Спостерігайте за змінами. Запишіть дисоціацію оцтової кислоти, зробіть висновок.
|
Послідовність дій |
Спостереження |
Хімічні рівняння. Йонні хімічні рівнння |
|
|
|
|
ВИСНОВОК _____________________________________________________________________________
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Лабораторний дослід №14. Взаємодія оцтової кислоти з металами, лугами і солями.
Інструктаж з БЖД.
Реактиви: розчин оцтової кислоти 6%, гранули цинку, розчин натрій гідроксиду, порошок кальці карбонату, розчин фенолфталеїну.
Обладнання та хімічний посуд: штатив з пробірками, скляна паличка, нагрівальний прилад.
14.1. У пробірку обережно помістіть гранулу цинку і налийте 1-2 мл розчину оцтової кислоти. Що відбувається? Якщо ознак реакції не помітите, вміст пробірки нагрійте, але не до кипіння. Зробіть висновок? Запишіть хімічні рівняння в молекулярному та йонному вигляді.
14.2. У пробірку налийте 2 мл. розчину натрій гідроксиду і добавте до нього декілька крапель фенолфталеїну. Доливайте в пробірку розчин оцтової кислоти. Зафіксуйте зовнішній ефект. Запишіть хімічні рівняння в молекулярному та йонному вигляді. Зробіть висновок.
14.3. У пробірку насипте трохи кальцій карбонату і долийте 1-2 мл. розчину оцтової кислоти. Що спостерігаєте? Запишіть хімічні рівняння в молекулярному та йонному вигляді. Зробіть висновок
|
Послідовність дій |
Спостереження |
Хімічні рівняння. Йонні хімічні рівнння |
Висновок |
|
14.1. Реакція оцтової кислоти з металом. |
|||
|
|
|
|
|
|
14.2. Реакція оцтової кислоти з лугом. |
|||
|
|
|
|
|
|
14.3. Реакція оцтової кислоти з сіллю |
|||
|
|
|
|
|
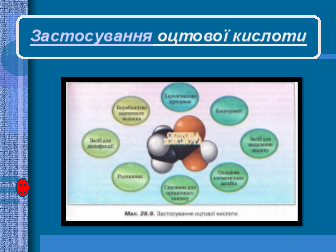
Застосування оцтової кислоти __________________________________________________________
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
- УВАГА НЕБЕЗПЕКА! Дія оцтової кислоти на біологічні тканини залежить від розведення її водою. Небезпечними вважаються розчини, в яких концентрація кислоти більше 30 %. Концентрована оцтова кислота здатна викликати хімічні опіки, які викликають некроз прилеглих тканин. Токсикологічні властивості оцтової кислоти не залежать від способу, яким вона була отримана. Смертельна доза складає приблизно 20 мл.
Домашнє завдання: 1. Опрацювати § 27. (П.П.Попель, Л.С.Крикля, Хімія – 9).
- І група учнів (оцінка 7-9), виконати вправи 239, 240. с. 162.
ІІ група учнів (оцінка 10-11), вправи 241, 245 с.162, 163.
3. Творче завдання: Написати казку “Подорож оцтової кислоти”.
Презентація до уроку: «Дослідження хімічних властивостей оцтової кислоти. Застосування оцтової кислоти».














![]()

ФОТОЗВІТ УРОКУ-ДОСЛІДЖЕННЯ «Дослідження хімічних властивостей оцтової кислоти. Застосування оцтової кислоти».










про публікацію авторської розробки
Додати розробку
